Перейти к:
Сравнительная оценка заболеваемости злокачественными новообразованиями шейки матки женщин, проживающих в регионах с различным уровнем радиационного, химического и сочетанного воздействия
https://doi.org/10.47470/0016-9900-2026-105-2-110-117
EDN: sinunn
Аннотация
Введение. Проживание на экологически неблагополучных территориях может значительно повышать вероятность возникновения злокачественных новообразований женской репродуктивной системы, в том числе шейки матки (ЗНОШМ).
Цель работы – определение влияния различных видов загрязнения окружающей среды (радиационного, химического и сочетанного) на формирование относительного риска и вероятность развития первичных онкологических патологий у женщин в возрасте от 41 года до 60 лет, имеющих диагностированную высоко-, низко- и умеренно дифференцированную форму ЗНОШМ, за двадцатилетний период (2000–2019 гг.).
Материалы и методы. Тест Шапиро – Уилка, U-критерий Манна – Уитни, относительный риск. Источники данных: Брянский областной онкологический диспансер, Роспотребнадзор, Ростехнадзор, Брянскстат.
Результаты. Установлено, что проживание в экологически неблагоприятных районах, подвергшихся химическому, радиоактивному или сочетанному воздействию, повышает риск развития у женщин ЗНОШМ (в том числе высоко-, низко- и умеренно дифференцированных форм). Относительный риск для женщин из этих районов по сравнению с женщинами из экологически благополучных зон составил 0,88 (95%-й доверительный интервал: 0,69–1,13). В районах радиоактивного загрязнения повышена вероятность развития высокодифференцированных и умеренно дифференцированных форм ЗНОШМ в сравнении с химически загрязнёнными территориями (значения относительного риска (ОР) варьируются от 1,16 до 1,39). При этом для низкодифференцированных форм ЗНОШМ не выявлено повышения ОР, который составил 1,03 (ДИ: 0,44–2,41). По сравнению с женщинами, живущими в районах, подверженных только химическому или радиоактивному загрязнению, у женщин, проживающих в зонах сочетанного воздействия, наблюдается более высокий относительный риск развития ЗНОШМ. Максимальные показатели ОР наблюдаются при высоко- и умеренно дифференцированных формах ЗНОШМ (от 1,4 до 2,19).
Ограничения исследования. Анализ первичной заболеваемости ЗНОШМ выполнен без учёта распределения по стадиям болезни и иммуногистохимического профиля.
Заключение. Исследование показало, что образ жизни и профилактика ВПЧ являются ключевыми факторами предупреждения ЗНОШМ. Расчёты относительного риска свидетельствуют о вероятном синергетическом эффекте воздействия радиационного и химического факторов на частоту заболеваемости низко- и особенно высоко- и умеренно дифференцированными формами ЗНОШМ в районах, где присутствовали оба вида загрязнения, по сравнению с территориями, подверженными только одному типу загрязнения.
Соблюдение этических стандартов. Использовалась обезличенная статистическая информация заболеваемости женщин ЗНОШМ на территории Брянской области с 2000 по 2019 г.
Вклад авторов:
Корсаков А.В. – анализ данных литературы, концепция и дизайн исследования, интерпретация полученных результатов, утверждение окончательного варианта статьи;
Крюкова А.Е. – поиск литературы, статистическая обработка, написание рукописи, редактирование и обсуждение статьи;
Трошин В.П. – анализ и интерпретация данных, написание текста, редактирование;
Милушкина О.Ю. – анализ данных литературы, анализ и интерпретация данных, редактирование;
Пивоваров Ю.П., Королик В.В. – анализ и интерпретация данных, редактирование.
Все соавторы – утверждение окончательного варианта статьи и ответственность за целостность всех её частей.
Благодарности. Авторы выражают благодарность А.И. Маклашову – главному врачу Брянского областного онкологического диспансера за предоставление обезличенной статистической информации о заболеваемости женщин злокачественными новообразованиями эндометрия в разрезе городов и районов Брянской области с 2000 по 2019 г.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов в связи с публикацией данной статьи.
Финансирование. Исследование не имело спонсорской поддержки.
Поступила: 15.04.2025 / Принята к печати: 26.06.2025 / Опубликована: 13.03.2026
Ключевые слова
Для цитирования:
Корсаков А.В., Крюкова А.Е., Трошин В.П., Милушкина О.Ю., Пивоваров Ю.П., Королик В.В. Сравнительная оценка заболеваемости злокачественными новообразованиями шейки матки женщин, проживающих в регионах с различным уровнем радиационного, химического и сочетанного воздействия. Гигиена и санитария. 2026;105(2):110-117. https://doi.org/10.47470/0016-9900-2026-105-2-110-117. EDN: sinunn
For citation:
Korsakov A.V., Kryukova A.E., Troshin V.P., Milushkina O.Yu., Pivovarov Yu.P., Korolik V.V. Comparative assessment of the incidence of malignant neoplasms of the uterine cervix in women residing in areas with different levels of radiation, chemical and combined exposure. Hygiene and Sanitation. 2026;105(2):110-117. (In Russ.) https://doi.org/10.47470/0016-9900-2026-105-2-110-117. EDN: sinunn
Введение
В соответствии с данными Международного агентства по изучению рака GLOBOCAN 2022, в мире ежегодно регистрируется ≈ 20 млн новых случаев злокачественных новообразований (ЗНО) и 9,7 млн смертей от ЗНО [1]. По оценкам экспертов, примерно каждый пятый мужчина или женщина в течение жизни сталкивается с диагнозом ЗНО. При этом примерно каждый девятый мужчина и каждая двенадцатая женщина умирают от ЗНО.
Согласно информации, предоставленной Российским научно-исследовательским онкологическим институтом им. П.А. Герцена, в 2023 г. рак шейки матки занял девятое место в рейтинге самых распространённых видов онкологических ЗНО: его доля составила 4,5% [2].
По данным исследователей [3–7], проживание в экологически неблагополучных условиях может существенно увеличивать риск развития ЗНО женской репродуктивной системы. Авторами установлена связь между загрязнением окружающей среды и гинекологическими опухолями, в том числе раком молочной железы, раком яичников и раком шейки матки [4].
Согласно результатам исследований [5], сжигание древесины и угля для отопления помещений увеличивает относительный риск смертности от рака шейки матки в 1,8–2,2 раза. В другом исследовании авторы выявили тесную связь повышенной концентрации свинца в окружающей среде и высокого риска заболеваемости женщин злокачественными новообразованиями шейки матки (без учёта случаев инфицирования HPV и нераковых) [6].
Как указано в источниках [8–10], во многих городах и районах Брянской области, затронутых Чернобыльской катастрофой, плотность радиоактивного загрязнения цезием-137 превышает установленные критерии отнесения территорий к зонам радиоактивного загрязнения (37 кБк/м²) [11, 12].
Согласно официальным сведениям*, в Брянской области в последние годы фиксируется рост выбросов газообразных поллютантов в атмосферу [13]. В некоторых районах региона население подвергается сочетанному воздействию радиоактивного и химического загрязнения [14–17]. Кроме того, из-за загрязнения окружающей среды ускоряются темпы мутационного процесса, что приводит к росту популяционного груза [18].
Цель исследования – определение относительного риска развития рака шейки матки и его частоты среди женщин в возрасте от 41 года до 60 лет, страдающих различными типами ЗНОШМ (высоко-, низко- и умеренно дифференцированные), в зависимости от уровня загрязнения окружающей среды в регионах проживания (радиоактивное, химическое и комбинированное) за 20-летний период.
Материалы и методы
Исследование плотности радиоактивного загрязнения территорий ¹³⁷Cs и ⁹⁰Sr после аварии на Чернобыльской АЭС проводили по информации, предоставленной в источнике [10], средние накопленные эффективные дозы облучения (СГЭД90) определяли по данным [12], уровень химического загрязнения атмосферного воздуха CO, NOx, SO2 и летучими органическими соединениями (ЛОС) – по данным [13].
На основании официальных данных Брянского областного онкологического диспансера [19] выполнен расчёт относительного риска (ОР) и частоты первичной заболеваемости высоко-, низко- и умеренно дифференцированными формами ЗНОШМ в зависимости от уровня химического и радиоактивного загрязнения за период 2010–2019 гг. Анализ гистологических форм ЗНОШМ проводился у женщин в возрасте от 41 года до 60 лет (376 случаев). Пересчёт абсолютных величин выполняли на 100 000 населения.
При статистическом анализе применяли критерии Шапиро – Уилка и Манна – Уитни, проведён анализ ОР с расчётом 95%-х доверительных интервалов.
Результаты
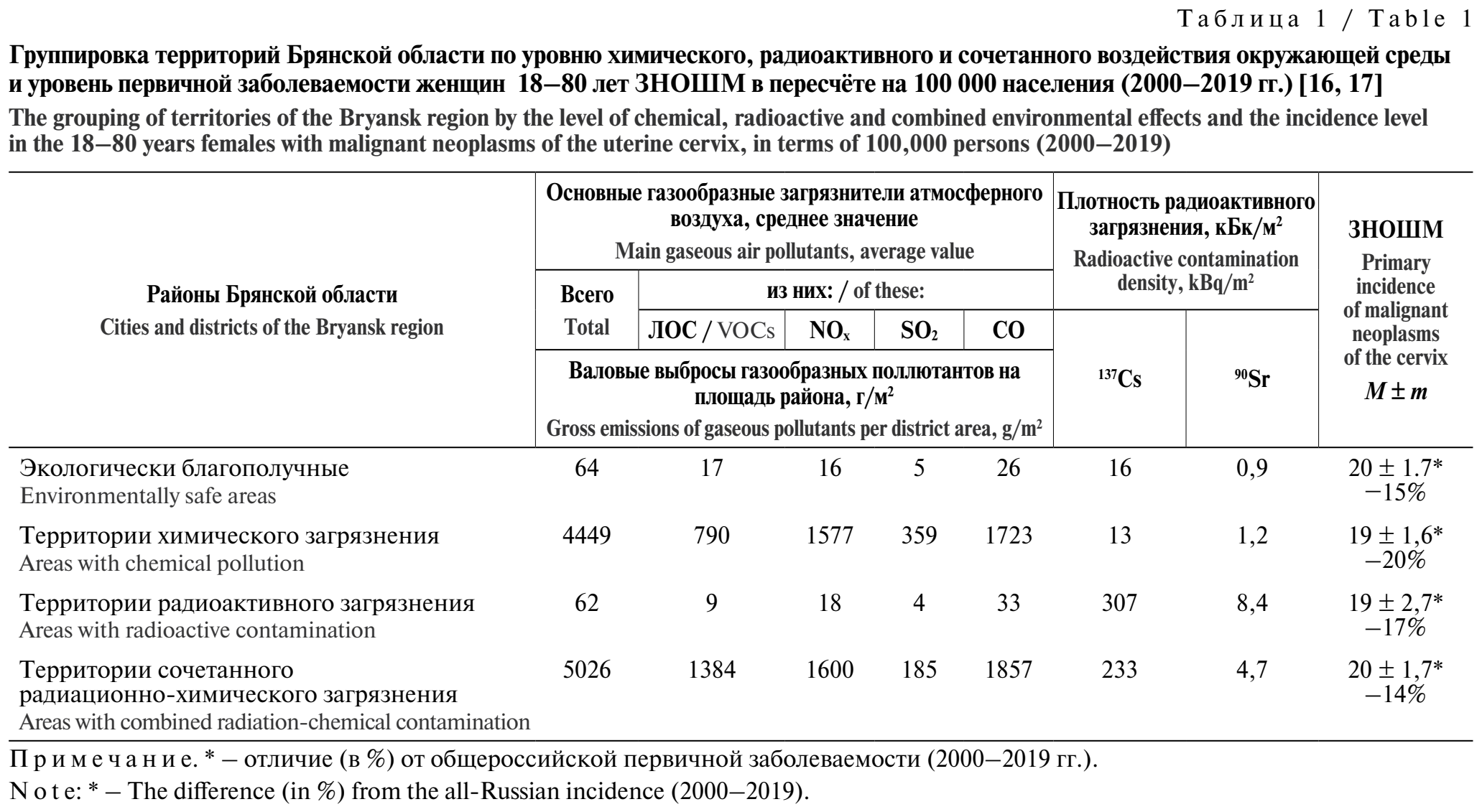
В Брянской области были выделены четыре группы территорий по степени радиоактивного и химического загрязнения, а также по частоте первичной заболеваемости ЗНОШМ в период с 2000 по 2019 г. Результаты этой классификации, изложенные в табл. 1, были ранее описаны в работах [16, 17].
Анализ частоты первичной заболеваемости женщин в возрасте от 41 года до 60 лет суммарно по высоко-, низко- и умеренно дифференцированным формам ЗНОШМ не выявил статистически достоверных различий между группами территорий независимо от экологических условий проживания (р > 0,05), результаты представлены в табл. 2. Уровень заболеваемости всеми формами ЗНОШМ колеблется от 8,5 ± 1,84 до 12,8 ± 3,27, из них: высокодифференцированными формами – от 2,2 ± 0,58 до 4,5 ± 1,23, умеренно дифференцированными формами – от 4,3 ± 0,92 до 9,9 ± 1,96 и низкодифференцированными формами – от 2,1 ± 0,51 до 3,3 ± 0,87 (см. табл. 2). Следует отметить, что частота высоко- и умеренно дифференцированных форм ЗНОШМ достигает максимальных значений в условиях сочетанного воздействия (4,5 ± 1,23 и 9,9 ± 1,96 соответственно), однако наибольшая частота низкодифференцированных форм ЗНОШМ зарегистрирована у женщин, проживающих в контрольных районах (3,3 ± 0,87).

Основываясь на данных, представленных в табл. 3, можно сделать вывод о том, что жительницы районов с неблагоприятной экологической обстановкой, в том числе территорий, подвергшихся химическому, радиоактивному и сочетанному воздействию, не имеют повышенного риска развития высоко-, низко- и умеренно дифференцированных форм ЗНОШМ по сравнению с женщинами, проживающими в экологически благополучных (контрольных) районах: ОР составляет 0,88 (ДИ: 0,69–1,13).

Тем не менее значения относительного риска по сравнению с контрольными районами значимо выше (р = 0,013) на территориях сочетанного загрязнения (ОР 1,51; ДИ: 1,09–2,1) и значимо ниже (р = 0,051) на территориях химического загрязнения (ОР 0,77; ДИ: 0,59–1), при этом в районах радиоактивного загрязнения не установлено повышенного риска (ОР 0,96; ДИ: 0,63–1,46), данные представлены в табл. 3.
Следует отметить, что значения относительного риска заболеваемости всеми формами ЗНОШМ на территориях сочетанного воздействия значимо выше (р = 0,001–0,027) относительно территорий как химического (ОР 1,96; ДИ: 1,48–2,58), так и радиоактивного (ОР 1,62; ДИ: 1,05–2,51) загрязнения. При этом величина риска формирования ЗНОШМ незначительно выше на территориях радиоактивного загрязнения относительно химического: ОР 1,20 (ДИ: 0,82–1,78), данные представлены в табл. 3.
Исследование, проведённое на основе данных табл. 4, не выявило роста ОР развития высокодифференцированных форм ЗНОШМ у женщин, проживающих в районах с различными видами загрязнения, по отношению к женщинам из контрольной группы. Относительный риск составил 0,85 (ДИ: 0,52–1,4). Тем не менее стоит подчеркнуть, что в зонах сочетанного загрязнения этот показатель достиг 1,47 (ДИ: 0,77–2,81), что превышает значение для контрольных зон, в то время как в зонах с химическим загрязнением ОР был равен 0,75 (ДИ: 0,44–1,25).

Необходимо отметить, что в зонах, подвергающихся сочетанному воздействию, у женщин наблюдается более выраженная тенденция к развитию высокодифференцированных форм ЗНОШМ по сравнению с зонами с химическим или радиоактивным загрязнением. Коэффициенты риска в таких зонах составляют 1,97 (ДИ: 1,14–3,42), что значительно превышает показатели для зон с химическим загрязнением (1,71; 0,71–4,11) и радиоактивным загрязнением.
Риск возникновения высокодифференцированных форм ЗНОШМ на территориях с радиоактивным загрязнением незначительно превышает риск на территориях с химическим загрязнением: ОР 1,16 (0,53–2,55), что отражено в табл. 4.
В отличие от анализа высокодифференцированных форм ЗНОШМ (см. табл. 3) анализ табл. 5 выявляет незначительное повышение ОР уровня первичной заболеваемости ЗНОШМ умеренно дифференцированных форм у женщин, проживающих в районах с неблагоприятной экологической обстановкой, в сравнении с контрольными районами: ОР 1,15 (ДИ: 0,79–0,7). Также значения риска относительно экологически благополучных территорий значимо выше (р = 0,001) на территориях с сочетанным загрязнением (ОР 2,12; ДИ: 1,32–3,41) и на территориях с радиоактивным загрязнением (ОР 1,35; ДИ: 0,75–2,44), при этом в районах с химическим загрязнением не установлено повышенного риска: ОР 0,97 (ДИ: 0,65–1,45), что отражено в табл. 5. На территориях, подвергающихся сочетанному воздействию, коэффициенты ОР достигают наибольших значений, превышая показатели территорий с химическим (ОР 2,19; ДИ: 1,51–3,17) и радиоактивным (ОР 1,57; ДИ: 0,89–2,78) загрязнением. Важно отметить, что риск развития умеренно дифференцированных форм ЗНОШМ на территориях с радиоактивным загрязнением выше, чем на территориях с химическим загрязнением (ОР 1,39; ДИ: 0,83–2,32), что показано в табл. 5.

Сравнительный анализ заболеваемости высоко- и умеренно дифференцированными формами ЗНОШМ (см. табл. 4, 5) и информация табл. 6 позволяют сделать вывод о том, что коэффициент ОР заболеваемости низкодифференцированными формами ЗНОШМ у женщин, проживающих на территориях, подвергшихся химическому, радиоактивному и сочетанному воздействию, меньше, чем в экологически благополучных районах: 0,66 (ДИ: 0,41–1,06).

В сравнении с контрольными районами коэффициенты ОР также демонстрируют снижение на территориях с химическим (ОР 0,62; ДИ: 0,38–1,02), радиоактивным (ОР 0,64; ДИ: 0,26–1,58) загрязнением и менее выражено в зонах сочетанного воздействия (ОР 0,9; ДИ: 0,45–1,81), что представлено в табл. 6. Важно подчеркнуть, что показатели относительного риска развития низкодифференцированных форм ЗНОШМ на территориях с сочетанным воздействием оказались выше, чем на территориях, подверженных только химическому (ОР 1,45; ДИ: 0,77–2,73) и радиоактивному (ОР 1,4; ДИ: 0,53–3,74) загрязнению.
При этом не выявлено повышения ОР частоты низкодифференцированных форм ЗНОШМ у женщин, проживающих на территориях радиоактивного загрязнения, относительно территорий химического загрязнения (ОР 1,03; ДИ: 0,44–2,41) (см. табл. 6).
Обсуждение
На возникновение злокачественных новообразований женской репродуктивной системы, в том числе ЗНОШМ, влияют многие факторы риска, ведущими из которых являются особенности образа жизни и отсутствие профилактики ВПЧ [20–24].
По данным [25], возникновение ЗНОШМ обусловлено персистирующей инфекцией, вызванной вирусом папилломы человека высокого онкогенного риска (HR-ВПЧ). Однако в их канцерогенезе важную роль играют и сопутствующие факторы, такие как курение, многоплодная беременность и длительное использование оральных гормональных контрацептивов.
Следует отметить, что авторами [26] выявлен высокий уровень инфицирования ВПЧ женщин репродуктивного возраста, проживающих на территориях, подвергшихся радиационному воздействию вследствие Чернобыльской катастрофы.
В другом исследовании [27] установлено, что сочетанное воздействие радиационного и химического загрязнения повышает риск развития низкодифференцированных форм злокачественных новообразований яичников по сравнению с зонами, имеющими только один из этих факторов загрязнения. Авторы исследования сделали вывод о синергетическом характере влияния радиационного и химического факторов.
Заключение
Исследование показало, что образ жизни и профилактика ВПЧ являются ключевыми факторами в предупреждении развития ЗНОШМ. Анализ не показал, что проживание в экологически неблагоприятных районах, подвергшихся химическому, радиоактивному или сочетанному воздействию, повышает риск развития ЗНОШМ (в том числе высоко-, низко- и умеренно дифференцированных форм) у женщин. Расчёты ОР свидетельствуют о вероятном синергетическом эффекте воздействия радиационного и химического факторов на частоту заболеваемости низко- и особенно высоко- и умеренно дифференцированными формами ЗНОШМ в районах, где присутствовали оба вида загрязнения, по сравнению с территориями, подверженными только одному виду загрязнения.
* Государственный доклад «О состоянии и об охране окружающей среды Российской Федерации в 2021 году». М.: Минприроды России; МГУ им. М.В. Ломоносова, 2023. 686 с. Государственный доклад 2021 (ecology-gosdoklad.ru).
Список литературы
1. Bray F., Laversanne M., Sung H., Ferlay J., Siegel R.L., Soerjomataram I., et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J. Clin. 2024; 74(3): 229–63. https://doi.org/10.3322/caac.21834
2. Каприн А.Д., Старинский В.В., Шахзадова А.О. Состояние онкологической помощи населению России в 2022 году. М.; 2023.
3. Иванова М.К., Шайфутдинова Г.М., Иванова А.Ю. Анализ взаимосвязи онкологической заболеваемости злокачественными новообразованиями репродуктивной системы у женщин Удмуртии от показателей загрязнения атмосферного воздуха. Международный журнал прикладных и фундаментальных исследований. 2018; (5–2): 339–43. https://elibrary.ru/uuxhue
4. Yu Q., Zhang L., Hou K., Li J., Liu S., Huang K., et al. Relationship between air pollutant exposure and gynecologic cancer risk. Int. J. Environ. Res. Public Health. 2021; 18(10): 5353. https://doi.org/10.3390/ijerph18105353
5. Liu T., Song Y., Chen R., Zheng R., Wang S., Li L. Solid fuel use for heating and risks of breast and cervical cancer mortality in China. Environ. Res. 2020; 186: 109578. https://doi.org/10.1016/j.envres.2020.109578
6. Zhang J., Nazeri S.A., Sohrabi A. Lead (Pb) exposure from outdoor air pollution: a potential risk factor for cervical intraepithelial neoplasia related to HPV genotypes. Environ. Sci. Pollut. Res. Int. 2022; 29(18): 26969–76. https://doi.org/10.1007/s11356-021-17608-x
7. Dutta S., Gorain B., Choudhury H., Roychoudhury S., Sengupta P. Environmental and occupational exposure of metals and female reproductive health. Environ. Sci. Pollut. Res. Int. 2022; 29(41): 62067–92. https://doi.org/10.1007/s11356-021-16581-9
8. Израэль Ю.А., Богдевич И.М. Атлас современных и прогнозных аспектов последствий аварии на Чернобыльской АЭС на пострадавших территориях России и Беларуси. М.-Минск: Инфосфера; 2009.
9. Яблоков А.В., Нестеренко В.Б., Нестеренко А.В., Преображенская Н.Е. Чернобыль: последствия Катастрофы для человека и природы. М.; 2016. https://elibrary.ru/wkdafj
10. Яхрюшин В.Н. Данные по радиоактивному загрязнению территории населённых пунктов Российской Федерации цезием-137, стронцием-90 и плутонием-239+240. Обнинск: НПО «Тайфун»; 2023.
11. Романович И.К., Брук Г.Я., Базюкин А.Б., Братилова А.А., Яковлев В.А. Динамика средних годовых и накопленных доз облучения взрослого населения Российской Федерации после аварии на Чернобыльской АЭС. Здоровье населения и среда обитания – ЗНиСО. 2020; (3): 33–8. https://doi.org/10.35627/2219-5238/2020-324-3-33-38 https://elibrary.ru/iufblc
12. Трапезникова Л.Н. Дозы облучения населения Брянской области от различных источников ионизирующего излучения за 2020 год (информационный справочник). Брянск; 2021.
13. Города и районы Брянской области (статистический сборник). Брянск; 2020.
14. Korsakov A.V., Geger E.V., Lagerev D.G., Pugach L.I., Mousseau T.A. De novo congenital malformation frequencies in children from the Bryansk region following the Chernobyl disaster (2000–2017). Heliyon. 2020; 6(8): e04616. https://doi.org/10.1016/j.heliyon.2020.e04616
15. Korsakov A.V., Golovleva A.A., Troshin V.P., Lagerev D.G., Pugach L.I. Ovarian malignancies frequency in the female population from the Bryansk region living in conditions of radioactive, chemical and combine contamination (2000–2020). Life (Basel). 2021; 11(11): 1272. https://doi.org/10.3390/life11111272
16. Корсаков А.В., Крюкова А.Е., Трошин В.П., Милушкина О.Ю., Лагерев Д.Г. Первичная заболеваемость злокачественными новообразованиями шейки матки населения, проживающего на экологически неблагополучных территориях (2000–2020 гг.). Гигиена и санитария. 2023; 102(1): 14–21. https://doi.org/10.47470/0016-9900-2023-102-1-14-21 https://elibrary.ru/davqrg
17. Korsakov A.V., Kryukova A.Е., Troshin V.P., Milushkina О.Y., Lagerev D.G. Cervical and endometrial cancer incidence in the female population from the Bryansk region living in conditions of chemical, radioactive and combined environmental contamination (2000–2020). Life. 2022; 12(10): 1488. https://doi.org/10.3390/life12101488 https://elibrary.ru/cbvhvy
18. Яблоков А.В. О концепции популяционного груза (обзор). Гигиена и санитария. 2015; 94(6): 11–4. https://elibrary.ru/uxzqrd
19. Первичная заболеваемость женского населения злокачественными новообразованиями яичников за 2000–2019 гг. Материалы Брянского областного онкологического диспансера. Брянск; 2021.
20. Rieck G., Fiander A. The effect of lifestyle factors on gynaecological cancer. Best Pract. Res. Clin. Obstet. Gynaecol. 2006; 20(2): 227–51. https://doi.org/10.1016/j.bpobgyn.2005.10.010
21. Wan Z., Zhao J., Xu L., Sun P., Shuai P., Li K., et al. Global and regional estimates of cervical cancer burden associated with human immunodeficiency virus infection from 1990 to 2019. J. Med. Virol. 2023; 95(6): e28891. https://doi.org/10.1002/jmv.28891
22. Ibrahim Khalil A., Mpunga T., Wei F., Baussano I., de Martel C., Bray F., et al. Age-specific burden of cervical cancer associated with HIV: A global analysis with a focus on sub-Saharan Africa. Int. J. Cancer. 2022; 150(5): 761–72. https://doi.org/10.1002/ijc.33841
23. Marino P., Mininni M., Deiana G., Marino G., Divella R., Bochicchio I., et al. Healthy lifestyle and cancer risk: modifiable risk factors to prevent cancer. Nutrients. 2024; 16(6): 800. https://doi.org/10.3390/nu16060800
24. Stelzle D., Tanaka L.F., Lee K.K., Ibrahim Khalil A., Baussano I., Shah A.S.V., et al. Estimates of the global burden of cervical cancer associated with HIV. Lancet Glob. Health. 2021; 9(2): e161–9. https://doi.org/10.1016/S2214-109X (20)30459-9
25. Bovo A.C., Pedrão P.G., Guimarães Y.M., Godoy L.R., Resende J.C.P., Longatto-Filho A., et al. Combined oral contraceptive use and the risk of cervical cancer: literature review. Rev. Bras. Ginecol. Obstet. 2023; 45(12): e818–24. https://doi.org/10.1055/s-0043-1776403
26. Крикунова Л.И., Киселева В.И., Мкртчян Л.С., Безяева Г.П., Панарина Л.В., Любина Л.В. и др. Папилломавирусная инфекция у женщин, подвергшихся радиоактивному воздействию вследствие аварии на Чернобыльской АЭС. Медико-биологические проблемы жизнедеятельности. 2017; (1): 146–53. https://elibrary.ru/uoqwpc
27. Головлева А.А., Корсаков А.В., Трошин В.П., Милушкина О.Ю., Пивоваров Ю.П., Королик В.В. и др. Сравнительная оценка заболеваемости злокачественными новообразованиями яичников женщин, проживающих на экологически неблагополучных территориях (2000–2019 гг.). Российский вестник гигиены. 2024; (4): 28–34. https://elibrary.ru/nuwkuw
Об авторах
Антон Вячеславович КорсаковРоссия
Доктор биол. наук, профессор каф. «Медицина катастроф», доцент ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Москва, Россия
e-mail: korsakov_anton@mail.ru
Анна Евгеньевна Крюкова
Россия
Аспирант каф. «Техносферная безопасность» ФГБОУ ВО БГТУ, 241035, Брянск, Россия
e-mail: kryukovaanna@bk.ru
Владислав Павлович Трошин
Россия
Доктор мед. наук, заслуженный врач РФ, профессор каф. «Техносферная безопасность» ФГБОУ ВО БГТУ, 241035, Брянск, Россия
e-mail: vptbr32@mail.ru
Ольга Юрьевна Милушкина
Россия
Доктор мед. наук, зав. каф. гигиены, доцент ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Москва, Россия
e-mail: olmilushkina@mail.ru
Юрий Петрович Пивоваров
Россия
Доктор мед. наук, профессор, академик РАН, заслуженный деятель науки РФ, профессор каф. гигиены педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Москва, Россия
Виктор Вячеславович Королик
Россия
Доктор мед. наук, профессор, профессор каф. гигиены ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Москва, Россия
Рецензия
Для цитирования:
Корсаков А.В., Крюкова А.Е., Трошин В.П., Милушкина О.Ю., Пивоваров Ю.П., Королик В.В. Сравнительная оценка заболеваемости злокачественными новообразованиями шейки матки женщин, проживающих в регионах с различным уровнем радиационного, химического и сочетанного воздействия. Гигиена и санитария. 2026;105(2):110-117. https://doi.org/10.47470/0016-9900-2026-105-2-110-117. EDN: sinunn
For citation:
Korsakov A.V., Kryukova A.E., Troshin V.P., Milushkina O.Yu., Pivovarov Yu.P., Korolik V.V. Comparative assessment of the incidence of malignant neoplasms of the uterine cervix in women residing in areas with different levels of radiation, chemical and combined exposure. Hygiene and Sanitation. 2026;105(2):110-117. (In Russ.) https://doi.org/10.47470/0016-9900-2026-105-2-110-117. EDN: sinunn
JATS XML








































