Перейти к:
Дезинвазия водных взвесей яиц гельминтов и цист кишечных простейших сверхвысокочастотным излучателем
https://doi.org/10.47470/0016-9900-2026-105-2-134-139
EDN: nlvnhf
Аннотация
Введение. Обеззараживание медицинских отходов при помощи сверхвысокочастотного (СВЧ) излучения в последнее время получает всё большее распространение за счёт удобства эксплуатации и низких затрат на обслуживание оборудования. Однако методики оценки эффективности дезинвазии предназначены для определения выживаемости паразитарных патогенов после длительной экспозиции в химических дезинфицирующих растворах и не подходят для оценки эффективности обеззараживания при воздействии кратковременного физического фактора. С целью расчёта эффективности дезинвазии с использованием СВЧ-установок нами апробирован упрощённый алгоритм на основе методики А.П. Симонова (МУК 4.2.2661–10).
Материалы и методы. В исследовании использованы водные взвеси яиц Enterobius vermicularis и Dibothriocephalus latus (Diphyllobothrium latum), полученных из половозрелых особей, и водные взвеси цист Entamoeba coli и яиц Opisthorchis felineus, полученных из фекалий пациентов. После обеззараживания при помощи СВЧ-установки в исследуемых и контрольных образцах проводили подсчёт и оценку жизнеспособности яиц гельминтов и цист простейших. Эффективность дезинвазии оценивали по числу жизнеспособных яиц или цист простейших в обработанной пробе в сравнении с контрольным образцом и рассчитывали в процентах.
Результаты. Эффективность дезинвазии в отношении возбудителей контактных паразитозов Enterobius vermicularis, Entamoeba coli при помощи СВЧ-установки составляет соответственно 98,68 и 99,86% по формуле А.П. Симонова и соответственно 99,33 и 100% по новой формуле. Эффективность дезинвазии при расчётах по обеим формулам сопоставима, интерпретация результатов совпадает и интерпретирована как высокоэффективная.
Ограничения исследования. Оценка эффективности дезинвазии по данной методике ограничивается видами Enterobius vermicularis, Diphyllobothrium latum, Opisthorchis felineus, Entamoeba coli и требует проверки на других гельминтах и простейших.
Заключение. Эффективность воздействия СВЧ-излучения для инвазионных стадий возбудителей с контактным механизмом передачи (Enterobius vermicularis, Entamoeba coli) составила 99–100%, что открывает перспективы применения СВЧ-излучения для дезинвазии и предотвращения передачи данных широко распространённых возбудителей паразитозов.
Соблюдение этических стандартов. Исследование не требует представления заключения комитета по биомедицинской этике или иных документов.
Вклад авторов:
Видманова М.В. – концепция и дизайн исследования, сбор материала и обработка данных, статистическая обработка, написание текста;
Лямин A.B., Халиулин А.В. – концепция и дизайн исследования, сбор материала и обработка данных;
Каюмов К.А. – обработка данных, написание текста, редактирование;
Козлов А.В. – концепция и дизайн исследования, сбор материала и обработка данных;
Яценко Т.В. – концепция и дизайн исследования;
Исматуллин Д.Д. – сбор материала и обработка данных.
Все соавторы – утверждение окончательного варианта статьи, ответственность за целостность всех её частей.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов в связи с публикацией данной статьи.
Финансирование. Исследование не имело финансовой поддержки.
Поступила: 07.02.2024 / Поступила после доработки: 06.10.2025 / Принята к печати: 02.12.2025 / Опубликована: 13.03.2026
Для цитирования:
Видманова М.В., Лямин А.В., Каюмов К.А., Козлов А.В., Халиулин А.В., Яценко Т.В., Исматуллин Д.Д. Дезинвазия водных взвесей яиц гельминтов и цист кишечных простейших сверхвысокочастотным излучателем. Гигиена и санитария. 2026;105(2):134-139. https://doi.org/10.47470/0016-9900-2026-105-2-134-139. EDN: nlvnhf
For citation:
Vidmanova M.V., Lyamin A.V., Kaiumov K.A., Kozlov A.V., Khaliulin A.V., Yatsenko T.V., Ismatullin D.D. Disinfection of aqueous suspensions of helminth eggs and intestinal protozoa cysts with an ultrahigh frequency radiator. Hygiene and Sanitation. 2026;105(2):134-139. (In Russ.) https://doi.org/10.47470/0016-9900-2026-105-2-134-139. EDN: nlvnhf
Введение
Ежегодно, по данным Всемирной организации здравоохранения, в мире регистрируется 100 млн новых случаев паразитарных инвазий, из них ≈ 2 млн – в нашей стране [1]. В структуре заболеваемости населения Российской Федерации паразитозы (гельминтозы и протозоозы) составляют 8,1% [2], наиболее распространены энтеробиоз и описторхоз. Для контактных паразитозов (например, энтеробиоз) факторами передачи являются предметы обихода, для биогельминтозов (например, описторхоз) – пищевые продукты, заражённые возбудителями через фекалии больного человека с участием промежуточных хозяев. Эффективная и нетрудоёмкая дезинвазия факторов передачи паразитарных возбудителей в окружающей и бытовой среде – актуальная задача дезинфектологии, особенно когда речь идёт о домашних очагах и обеспечении санитарно-противоэпидемического режима в медицинских организациях и организованных коллективах. Для паразитарных возбудителей в зависимости от объекта используются различные методы дезинвазии. Способы оценки эффективности дезинвазии (овоцидной и протистоцидной активности) различных дезинфицирующих средств представлены в нормативном документе МУК 4.2.2661–10 «Методы санитарно-паразитологических исследований». Они предусматривают расчёт оптимальных эффективных концентраций и времени экспозиции химических веществ. Это не вполне применимо для оценки эффективности дезинвазии при воздействии физических факторов.
На современном этапе основными методами обеззараживания медицинских, лабораторных и иных отходов являются физический (автоклавирование, СВЧ-облучение) и химический [3]. В изученных авторами публикациях проблема дезинвазии объектов внешней среды физическими способами отражена незначительно, большинство работ посвящено химическим способам [4–7]. Существуют исследования, направленные на изучение альтернативного способа физической дезинфекции – СВЧ-облучения, однако в основном в отношении бактериальных агентов [8–10]. Отчасти это объясняется отсутствием отдельного способа оценки эффективности овоцидного и протистоцидного действия физических факторов. Также причиной может быть трудоёмкость паразитологической оценки жизнеспособности паразитарных возбудителей и сложность их накопления для масштабных экспериментальных исследований.
Обеззараживание медицинских отходов при помощи сверхвысокочастотного (СВЧ) излучения в последнее время получает всё большее распространение за счёт удобства эксплуатации и небольших затрат на обслуживание оборудования, однако оценка эффективности дезинвазии с применением такой методики требует корректировки для возбудителей паразитарных болезней.
Цель исследования – оценка эффективности обеззараживания стандартного режима СВЧ-излучателя в отношении инвазионных стадий возбудителей паразитозов, контаминирующих объекты окружающей среды, и корректировка методики оценки эффективности дезинвазии для физических факторов.
Материалы и методы
Экспериментальные исследования проведены в отделении паразитологических исследований микробиологической лаборатории, имеющей лицензию на работу с ПБА III–IV групп патогенности.
Возбудители паразитозов, использованные в эксперименте, получены от пациентов, исследованы и идентифицированы до биологического вида согласно МУК 4.2.3145–13 «Лабораторная диагностика гельминтозов и протозоозов».
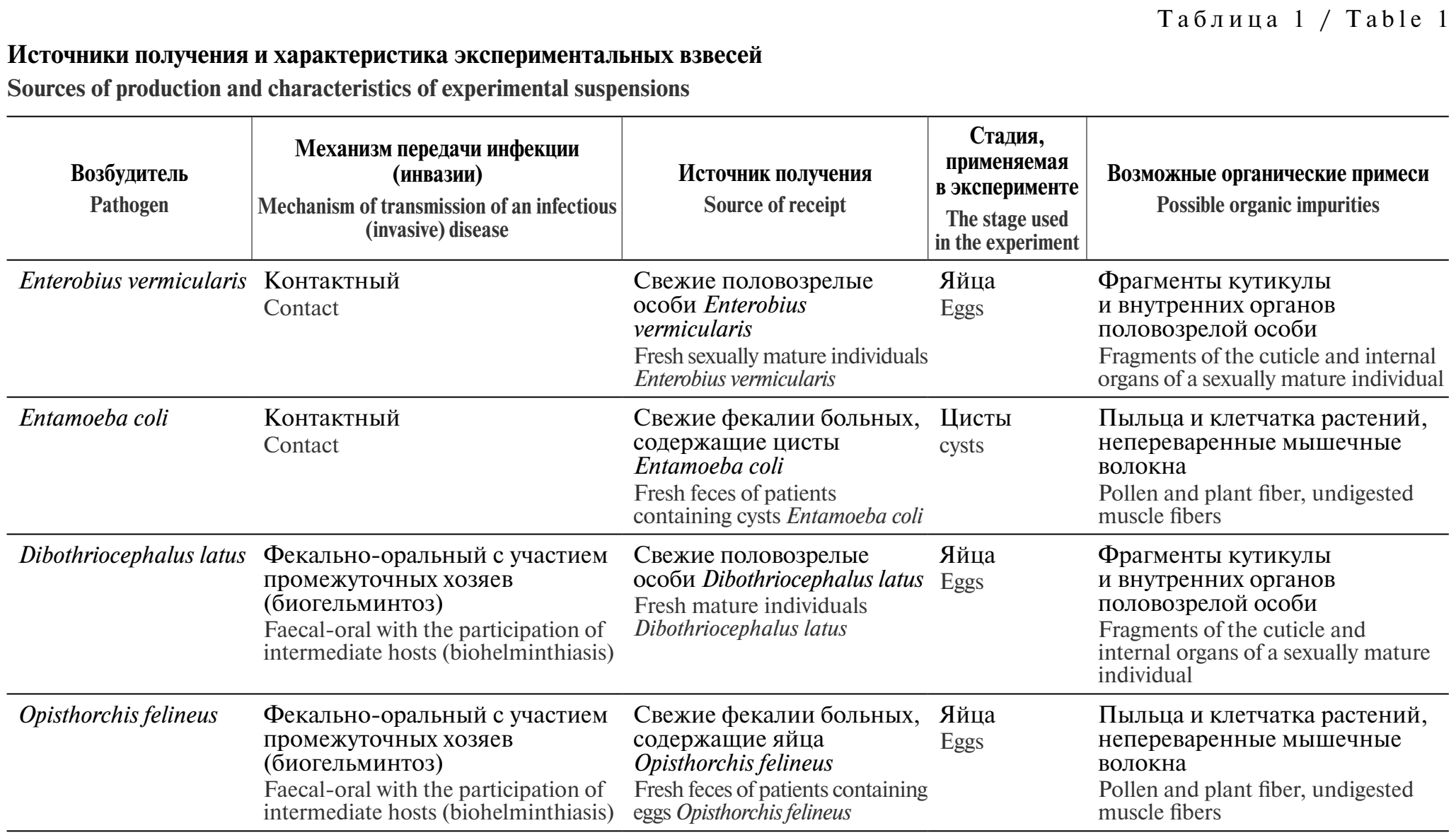
Непосредственно для исследования использовали водные взвеси яиц Enterobius vermicularis и Dibothriocephalus latus (Diphyllobothrium latum), полученных из свежих половозрелых особей, и водные взвеси цист Entamoeba coli и яиц Opisthorchis felineus, полученных путём седиментационного обогащения из свежих фекалий пациентов. Взвеси яиц (цист) содержали также примеси органических веществ как погрешность очистки первичных биоматериалов. Систематизированная информация представлена в табл. 1.
Готовые взвеси яиц (цист) возбудителей паразитозов после тщательного многократного перемешивания дозатором во избежание осаждения быстро распределяли на три термоустойчивые пробирки по 1 мл в каждой. Первую из пробирок подвергали дезинвазии при помощи СВЧ-установки «УОМО-01/150» (время экспозиции 60 мин, мощность СВЧ-излучения 600 Вт), вторую подвергали дезинвазии путём автоклавирования (температура плюс 132 °С, экспозиция 20 мин), третью оставляли в качестве контрольной пробы. После облучения в исследуемых и контрольных образцах проводили подсчёт и оценку жизнеспособности яиц гельминтов и цист простейших.
Количество яиц и цист в экспериментальных взвесях не уравнивалось между изучаемыми возбудителями, так как в реальных условиях контаминация ими объектов окружающей среды вариабельна, а для заражения восприимчивого организма достаточно единичных инвазионных стадий. Минимальное содержания яиц и цист в экспериментальных взвесях было обусловлено яйцепродукцией половозрелых особей, степенью инвазии пациентов, от которых получен биоматериал, и количеством полученного биоматериала (фекалий). Максимальное содержание яиц и цист в экспериментальных взвесях зависело от сохранности нативных взвесей. Содержание яиц (цист) в экспериментальных взвесях соответствует обычной (случайной) контаминации предметов обихода и имеет значение только для математических расчётов в эксперименте. Количественное содержание яиц и цист в экспериментальных взвесях оценивали методом световой микроскопии нативных препаратов при увеличении ×100. Нативные препараты готовили из взвесей таким образом, чтобы паразитарные объекты располагались в один слой разрозненно и легко подвергались визуальному учёту при зигзагообразной последовательной микроскопии всей площади нативного препарата.
Методы оценки жизнеспособности были подобраны для каждого возбудителя и описаны в данной статье в соответствии с рекомендациями и терминологией МУК 4.2.2661–10 «Методы санитарно-паразитологических исследований».
Жизнеспособность яиц Enterobius vermicularis оценивали с помощью световой микроскопии (×100, ×400) неокрашенных препаратов (МУК 4.2.2661–10, п. 15.1) и люминесцентной микроскопии (×100, ×400) препаратов, окрашенных акридиновым оранжевым, в разведении 1 : 500 (МУК 4.2.2661–10, п. 15.5). При световой микроскопии у живых яиц Enterobius vermicularis наблюдались характерные морфологические особенности (размеры 50–60 × 20–30 мкм, D-образная форма, асимметричность, двухконтурная оболочка). Погибшие яйца имели видимые дефекты (сильное изменение формы, разрыв оболочки). При люминесцентной микроскопии оболочка яиц имела оранжево-красный цвет, внутреннее содержимое у жизнеспособных яиц имело тусклое серо-зелёное окрашивание, а у погибших – «горящее» светло-зелёное.
Жизнеспособность цист Entamoeba coli оценивали с помощью световой микроскопии (×100, ×400) препаратов, окрашенных акридиновым оранжевым, в разведении 1 : 500 (МУК 4.2.2661–10, п. 16.2). При световой микроскопии у цист Entamoeba coli наблюдались характерные морфологические особенности (цисты кругло-овальной и круглой формы диаметром 15–20 мкм, симметричные, с 6–8 ядрами, чёткой тонкой оболочкой, мелкозернистой цитоплазмой без деления на экто- и эндоплазму). У погибших яиц наблюдались видимые дефекты (неправильная форма, разрыв оболочки, отсутствие чётких внутренних структур при сохранении узнаваемых формы и размеров). При люминесцентной микроскопии (×400) у живых цист Entamoeba coli наблюдалось свечение оболочки оранжевым цветом, а цитоплазма не прокрашивалась. У погибших цист цитоплазма и оболочка окрашивалась в красный или красно-оранжевый цвета.
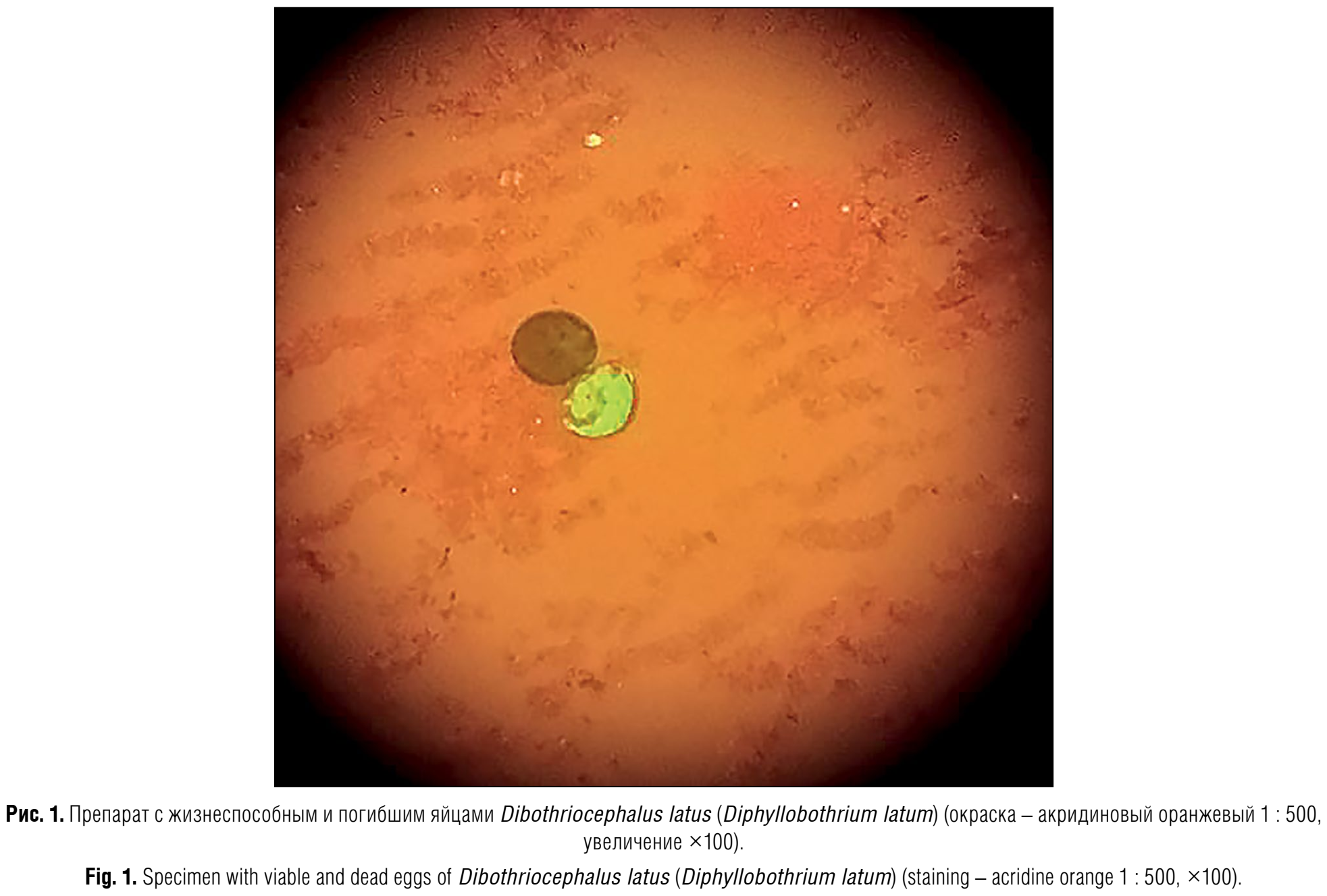
Жизнеспособность яиц Dibothriocephalus latus (Diphyllobothrium latum) оценивали с помощью световой микроскопии (×100) неокрашенных препаратов (МУК 4.2.2661–10, п. 15.1) и люминесцентной микроскопии (×100, ×400) препаратов, окрашенных акридиновым оранжевым (1 : 500) (МУК 4.2.2661–10, п. 15.5). У яиц Diphyllobothrium latum при световой микроскопии наблюдались характерные морфологические особенности (размеры 65–70 × 40–45 мкм, кругло-овальная форма, симметричность, тонкая оболочка, наличие слаборазличимой крышечки и бугорка на противоположных полюсах яйца). При люминесцентной микроскопии жизнеспособные яйца имели тусклый тёмно-зелёный или серо-зелёный цвет, а погибшие – «горящий» светло-зелёный цвет (рис. 1, см. на вклейке).
Жизнеспособность яиц Opisthorchis felineus оценивали с помощью световой микроскопии (×100, ×400) неокрашенных препаратов (МУК 4.2.2661–10, п. 15.1) и при люминесцентной микроскопии (×100, ×400). У яиц O. felineus при световой микроскопии наблюдались характерные морфологические особенности (размеры 25–27 × 15 мкм, семечковидная форма, небольшая асимметричность, тонкая оболочка, наличие крышечки на более узком полюсе и бугорка на противоположном более широком полюсе). При люминесцентной микроскопии живые яйца не люминесцировали, а погибшие имели желтовато-зелёный цвет.
Для оценки эффективности дезинвазии первоначально расчёты выполняли по формуле А.П. Симонова, рекомендованной для химических методов дезинвазии (МУК 4.2.2661–10, п. 17.2), с длительной экспозицией. Согласно данной формуле (1), в эксперименте фиксировали следующие параметры:
ОЭС = 100 – (a1 · c1/a2 · c2) · 100 – (P1 – P2) / n, (1)
где ОЭС – овоцидная (протистоцидная) эффективность препарата (%); a1 – количество живых яиц (цист) в опыте; a2 – количество живых яиц (цист) в контроле; c1 – количество яиц (цист), взятых для определения их жизнеспособности, в опыте; c2 – количество яиц (цист), взятых для определения их жизнеспособности, в контроле; P1 – процент погибших яиц (цист) в опыте; P2 – процент живых яиц (цист) в опыте; n – количество яиц (цист) во взвеси, взятой для испытания в опыте.
Для проведения данных расчётов и оценки эксперимента рекомендовано (МУК 4.2.2661–10, п. 17.2) использовать значительные количества свежеполученных паразитарных возбудителей на стадии яиц (цист) – более 1000. Рекомендация обусловлена тем, что некоторая часть яиц (цист) станет нежизнеспособной во время длительной экспозиции в результате естественной гибели, и только оставшиеся, возможно, погибнут от воздействия изучаемых химических средств, но при этом могут сохранить свои внешние признаки [6]. Оценка жизнеспособности яиц (цист) проводится путём микроскопии с оценкой морфологических свойств и степени восприятия красителя у каждого паразитарного объекта, что достаточно трудоёмко, поэтому для определения жизнеспособности больших количеств яиц (цист) в формуле А.П. Симонова предусмотрено изучение выборки из опыта и выборки из контроля.
Предварительно проведённые экспериментальные исследования показали, что после воздействия СВЧ-излучения сохранность яиц (цист) вариабельна: некоторые сохраняют свои морфологические признаки, легко идентифицируются и подвергаются количественному учёту, другие значительно деструктурируются, распадаются на фрагменты, что затрудняет их подсчёт, остальные яйца (цисты) вовсе не обнаруживаются в опытной взвеси из-за сильного разрушения. Таким образом, после проведения эксперимента возможно корректно подсчитать только уцелевшие яйца (цисты), а не все подвергавшиеся воздействию, как это делается в экспериментах по оценке эффективности дезинвазии химическими веществ. Поэтому для эксперимента готовили взвеси свежеполученных яиц (цист) с одинаковым количеством в опытных и контрольных образцах. При таком подходе некоторые параметры формулы Симонова А.П. (n, c1, a2) становились заведомо равными друг другу, что позволило упростить формулу. Оценку жизнеспособности всех сохранившихся паразитарных объектов в опытных и контрольных взвесях проводили микроскопически.
Далее эффективность дезинвазии рассчитывали при помощи упрощённой методики по формуле (2) :
ОЭН = 100% – (a1 / c2) · 100%, (2)
где ОЭН – эффективность дезинвазии для физического фактора; a1 – количество живых яиц (цист) в опыте; c2 – количество яиц (цист), взятых для определения их жизнеспособности, в контроле.
Статистический анализ проводили с использованием программы StatTech v. 4.8.11 (ООО «Статтех», Россия, номер регистрации 2020615715, дата регистрации 29.05.2020 г.; включена в единый реестр российских программ для электронных вычислительных машин и баз данных (запись № 14167 от 11.07.2022 г.)).
В ходе статистического анализа количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Шапиро – Уилка. Количественные показатели, выборочное распределение которых соответствовало нормальному, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD). В качестве меры репрезентативности для средних значений указывались границы 95%-го доверительного интервала (95% ДИ).
Сравнение двух групп по количественному показателю, распределение которого в каждой из групп соответствовало нормальному, при условии равенства дисперсий выполнялось с помощью t-критерия Стьюдента. Различия считались статистически значимыми при p < 0,05.
Результаты
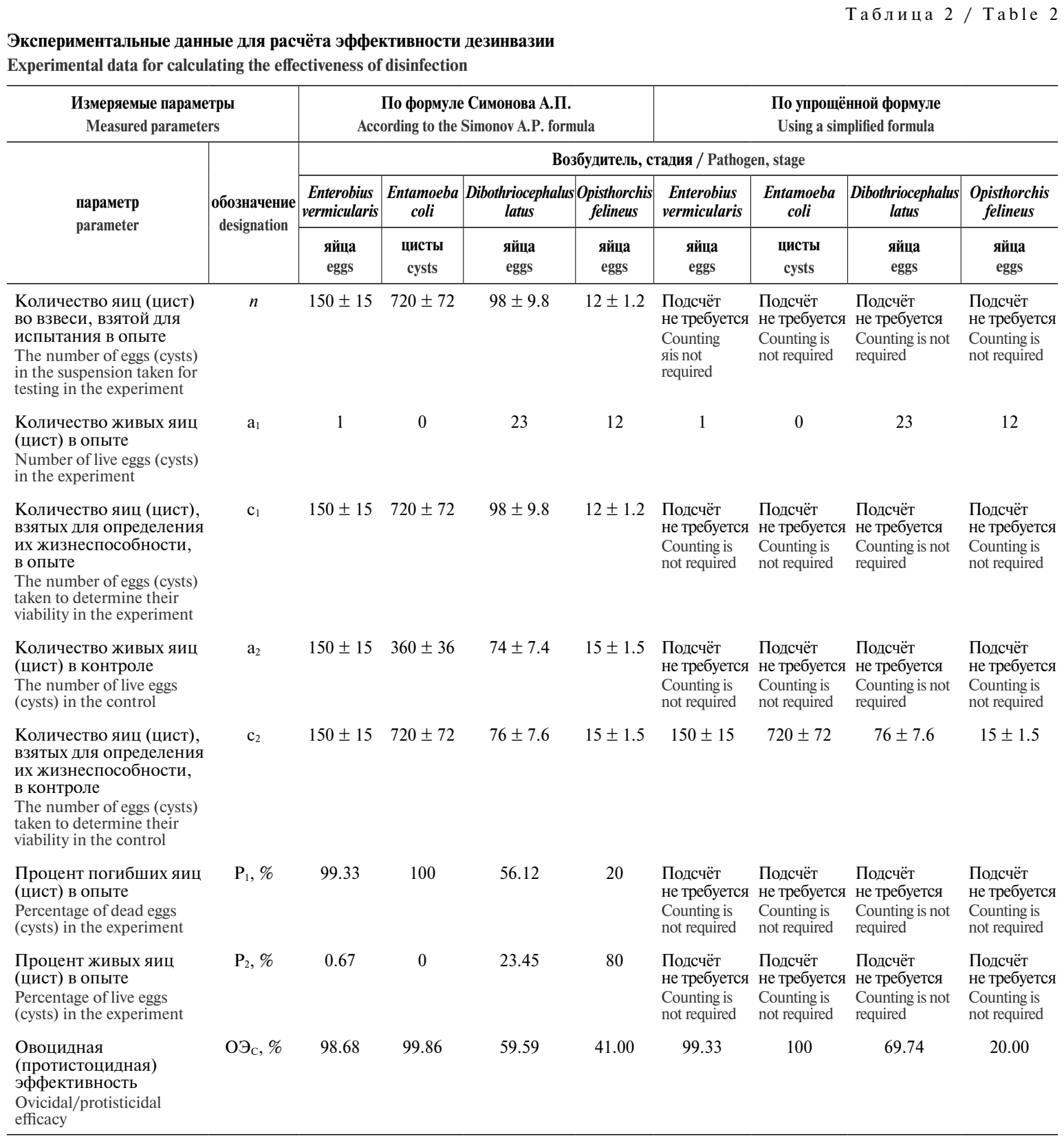
После дезинвазии проб в исследуемых и контрольных образцах проводили подсчёт и оценку жизнеспособности яиц гельминтов и цист простейших каждого возбудителя согласно вышеуказанным методикам. Полученные экспериментальные данные представлены в табл. 2 в соответствии с параметрами формулы Симонова А.П., рекомендованной в МУК 4.2.2661–10, п. 17.2.
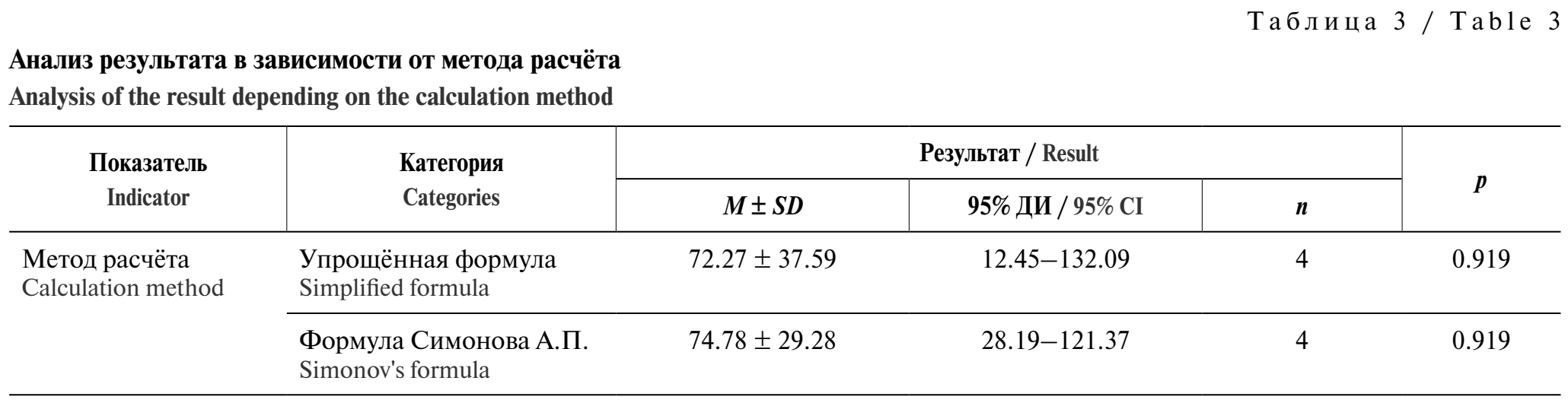
Проведён анализ количественного значения ОЭ (%) в зависимости от метода расчёта (формулы (1), (2)). При сравнении результатов нам не удалось выявить статистически значимых различий (p = 0,919), используемый метод – t-критерий Стьюдента (табл. 3; рис. 2, см. на вклейке).
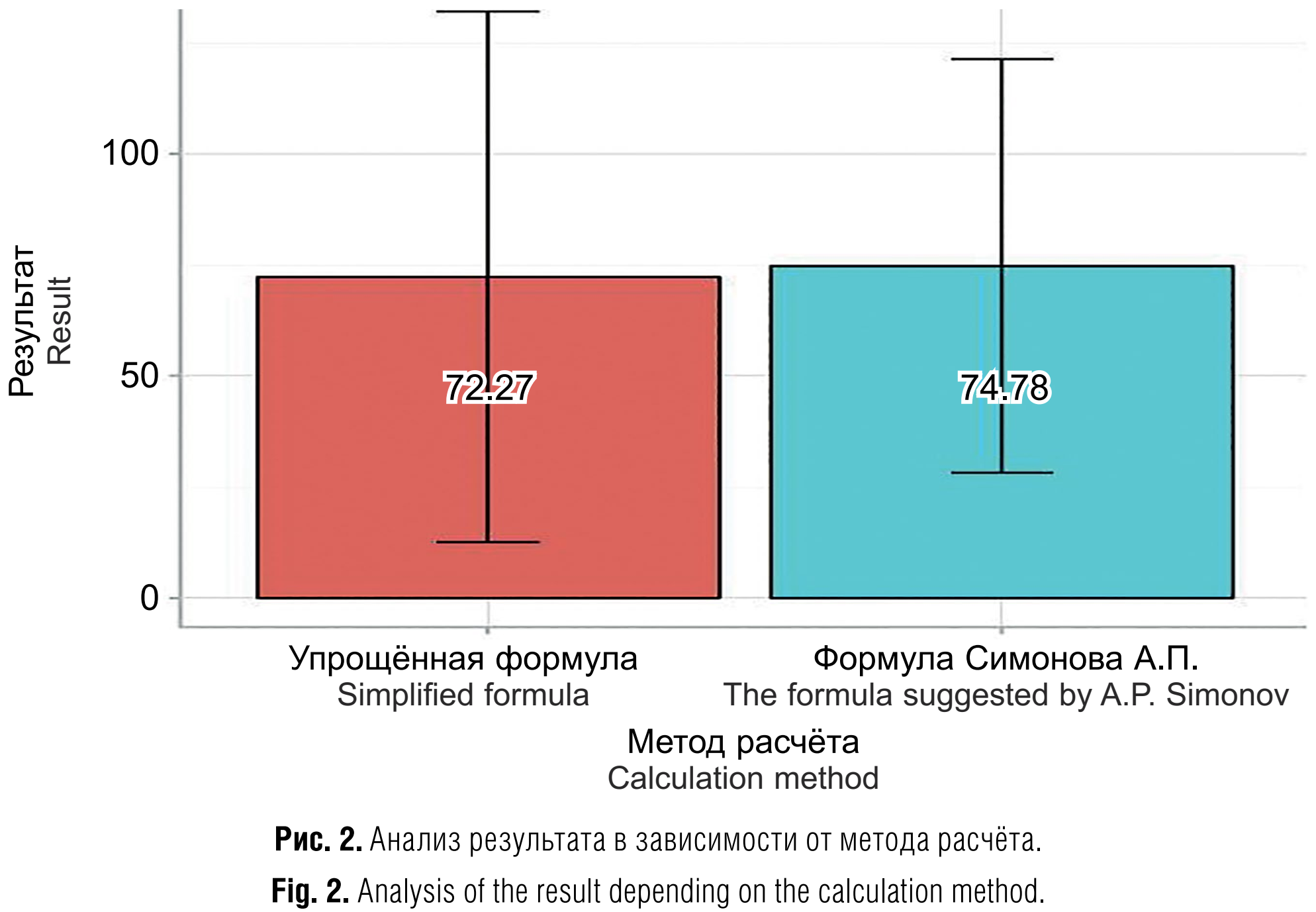
Таким образом, овоцидная (протистоцидная) эффективность в отношении изучаемых возбудителей паразитозов, рассчитанная с помощью формулы (1) Симонова А.П., сопоставима с эффективностью, рассчитанной по упрощённой формуле (2).
Согласно МУК 4.2.2661–10 (п. 17.1), овоцидная (протистоцидная) эффективность признаётся высокой при значении 90–100%; удовлетворительной – при 60–90%; неудовлетворительной – при значении менее 60%.
Согласно данным табл. 2, эффективность дезинвазии с использованием СВЧ-излучения для возбудителей с контактным механизмом передачи (Enterobius vermicularis, Entamoeba coli) составила 99–100%, а для возбудителей природно-очаговых биогельминтозов (Diphyllobothrium latum, Opisthorchis felineus) – 20–68%.
Таким образом, дезинвазию СВЧ-облучением в отношении паразитарных агентов с контактным механизмом передачи (Enterobius vermicularis, Entamoeba coli) можно считать высокоэффективной.
Для биогельминтозов Diphyllobothrium latum и Opisthorchis felineus эффективность дезинвазии проб при стандартном режиме работы СВЧ-установки, рассчитанная по двум формулам, в количественном выражении существенно различается, но интерпретирована одинаково как неудовлетворительная. Поэтому для яиц биогельминтов такая дезинвазия может рассматриваться только как дополнительная в комплексе противоэпидемических мер.
Обсуждение
В данном исследовании наибольший интерес представляла оценка дезинвазионной эффективности стандартного режима СВЧ-излучателя в отношении контактных паразитозов, а именно их инвазионных стадий (Enterobius vermicularis и Entamoeba coli). Возбудители биогельминтозов Opisthorchis felineus и Diphyllobothrium latum на стадии яйца не являются инвазионными для человека и рассматривались в рамках данного исследования дополнительно как примеры другого механизма передачи паразитарных болезней.
Дезинвазия объектов окружающей среды на современном этапе представляет собой актуальную задачу, что связано с высокой устойчивостью паразитарных агентов к агрессивным факторам, особенно это касается инвазионных для человека стадий [7]. Современные физические способы дезинвазии (механический – удаление с поверхностей во время выколачивания, встряхивания, смывания, осаждения и др.; термический – кипячение, сжигание, обжигание, фламбирование, замораживание; автоклавирование) широко применяются на практике, однако часто имеют ограничения, связанные с сохранением свойств объекта, подвергаемого дезинвазии, тогда как СВЧ-излучение относится к щадящим воздействиям, что заслуживает внимания. Согласно полученным данным, эффективность дезинвазии СВЧ-излучением оказалась сопоставима при расчётах по формуле Симонова А.П. и с помощью предложенной нами упрощённой методики.
Высокая эффективность дезинвазии СВЧ-облучением позволяет судить о перспективах его применения для бытовых и некоторых медицинских изделий многократного применения, не подлежащих кипячению, замачиванию, фламбированию (игрушки, посуда, пластиковые наконечники и др.).
Поскольку в Российской Федерации энтеробиоз является самым распространённым гельминтозом, а факторы его передачи – многочисленные предметы обихода, на поверхности которых яйца Enterobius vermicularis при комнатной температуре могут оставаться жизнеспособными неопределённо долго, появление дополнительного эффективного и доступного метода дезинвазии объектов окружающей среды открывает новые возможности в борьбе с этим гельминтозом.
Ограничения исследования. Оценка эффективности дезинвазии с применением данной методики ограничивается видами Enterobius vermicularis, Diphyllobothrium latum, Opisthorchis felineus, Entamoeba coli и требует проверки на других гельминтах и простейших.
Заключение
Альтернативные способы дезинвазии объектов окружающей среды с применением современных физических технологий имеют высокую практическую значимость для медицинских и иных учреждений, но требуют одновременной разработки соответствующих методов оценки эффективности обеззараживания. На основе оценки эффективности химического способа дезинвазии разработана упрощённая методика оценки эффективности дезинвазии с помощью кратковременного физического воздействия (на примере СВЧ-излучения). Пригодность методики для оценки дезинвазии агентов контактных паразитозов подтверждена экспериментально с использованием модельных взвесей инвазивных форм возбудителей.
Высокая эффективность СВЧ-излучения в отношении инвазионных стадий Enterobius vermicularis открывает перспективы профилактики и противоэпидемических мероприятий в отношении энтеробиоза – наиболее распространённого в Российской Федерации гельминтоза.
Список литературы
1. Асланова М.М., Кузнецова К.Ю., Загайнова А.В., Синицына О.О., Шихбабаева Ф.М., Рудинский А.В. Основные проблемы эпидемиологического мониторинга за паразитозами на территории Российской Федерации. Здоровье населения и среда обитания – ЗНиСО. 2018; (3): 29–31. https://doi.org/10.35627/2219-5238/2018-300-3-29-31 https://elibrary.ru/ytztjk
2. Чудиновских С.А., Мирзоева Р.К. Эпидемиология распространения паразитов. В кн.: Здоровье нации в XXI веке. Материалы II Всероссийской научно-практической конференции. Краснодар; 2021: 151–7. https://elibrary.ru/elkkke
3. Долбин Д.А., Хайруллин Р.З. Анализ эффективности использования современных средств для дезинвазии. Вестник Казанского технологического университета. 2015; 18(16): 314–5. https://elibrary.ru/ungukz
4. Ахмед Н.К., Фёдорова Л.С. Методы изучения и оценки эффективности химических средств дезинфекции для обеззараживания воды от возбудителей паразитарных инфекций (обзор литературы). Дезинфекционное дело. 2019; (4): 25–37. https://doi.org/10.35411/2076-457X-2019-4-25-37 https://elibrary.ru/nyoova
5. Долбин Д.А., Хайруллин Р.З. Изучение влияние ряда химических, физических и биологических факторов окружающей среды на эффективность дезинвазии помещений. Вестник Казанского технологического университета. 2015; 18(15): 261–4. https://elibrary.ru/ulrpzb
6. Романенко Н.А., Падченко И.К., Чебышев Н.В. Санитарная паразитология: Руководство для врачей. М.: Медицина; 2000.
7. Ursache A.L., Mircean V., Dumitrache M., Andrei S., Ştefănuţ L., Cozma V., et al. Is routine disinfection efficient in preventing contamination with Toxocara canis eggs? J. Helminthol. 2019; 94: e60. https://doi.org/10.1017/S0022149X1900052X
8. Германчук В.Г., Семакова А.П., Лобовикова О.А., Гордеева М.В., Шавина Н.Ю., Морозов К.М. и др. Эффективность установки СВЧ-излучения «СТЕРИУС 60» для обеззараживания объектов, контаминированных ПБА I–IV групп, при работе с инфицированными биомоделями. Проблемы особо опасных инфекций. 2020; (4): 53–8. https://doi.org/10.21055/0370-1069-2020-4-53-58 https://elibrary.ru/jbbutw
9. Liu J., Li H., Liu Z., Meng X., He Y., Zhang Z. Study on the process of medical waste disinfection by microwave technology. Waste Manag. 2022; 150: 13–9. https://doi.org/10.1016/j.wasman.2022.06.022
10. Liu L., Wang N., Laghari A.A., Li H., Wang C., Zhao Z., et al. A review and perspective of environmental disinfection technology based on microwave irradiation. Curr. Pollut. Rep. 2023; 9(1): 46–59. https://doi.org/10.1007/s40726-022-00247-2
Об авторах
Мария Владимировна ВидмановаРоссия
Врач-бактериолог микробиологической лаб. ФБУЗ «ЦГиЭ в Самарской области», 443079, Самара, Россия
e-mail: maria.vidmanova17@yandex.ru
Артем Викторович Лямин
Россия
Доктор мед. наук, директор НОПЦ ГЛТ, ФГБОУ ВО СамГМУ Минздрава России, 443099, Самара, Россия.
Карим Аскерович Каюмов
Россия
Специалист НОПЦ ГЛТ, ФГБОУ ВО СамГМУ Минздрава России, 443099, Самара, Россия
e-mail: k.a.kayumov@samsmu.ru
Андрей Владимирович Козлов
Россия
Зав. лаб. НОПЦ ГЛТ, ФГБОУ ВО СамГМУ Минздрава России, 443099, Самара, Россия.
Алмаз Вадимович Халиулин
Россия
Зав. лаб. НОПЦ ГЛТ, ФГБОУ ВО СамГМУ Минздрава России, 443099, Самара, Россия.
Татьяна Вадимовна Яценко
Россия
Врач-вирусолог микробиологической лаборатории ФБУЗ «ЦГиЭ в Самарской области», 443079, Самара, Россия.
Данир Дамирович Исматуллин
Россия
Канд. мед. наук, зав. лаб. НОПЦ ГЛТ, ФГБОУ ВО СамГМУ Минздрава России, 443099, Самара, Россия.
Рецензия
Для цитирования:
Видманова М.В., Лямин А.В., Каюмов К.А., Козлов А.В., Халиулин А.В., Яценко Т.В., Исматуллин Д.Д. Дезинвазия водных взвесей яиц гельминтов и цист кишечных простейших сверхвысокочастотным излучателем. Гигиена и санитария. 2026;105(2):134-139. https://doi.org/10.47470/0016-9900-2026-105-2-134-139. EDN: nlvnhf
For citation:
Vidmanova M.V., Lyamin A.V., Kaiumov K.A., Kozlov A.V., Khaliulin A.V., Yatsenko T.V., Ismatullin D.D. Disinfection of aqueous suspensions of helminth eggs and intestinal protozoa cysts with an ultrahigh frequency radiator. Hygiene and Sanitation. 2026;105(2):134-139. (In Russ.) https://doi.org/10.47470/0016-9900-2026-105-2-134-139. EDN: nlvnhf
JATS XML








































