Перейти к:
Биологическая активность левоглюкозенона и его производных (аналитический обзор)
https://doi.org/10.47470/0016-9900-2026-105-2-207-213
EDN: flrmmn
Аннотация
Введение. Левоглюкозенон (ЛГ) – енон углеводной природы, получаемый кислотным пиролизом целлюлозы. С учётом мощного синтетического потенциала и доступности ЛГ мы посчитали интересным изучить его возможности как платформы в синтезе широкого круга хиральных органических молекул с целью выявления биологической активности полученных производных.
Материалы и методы. Прогнозирование биологических свойств ЛГ и его синтезированных в лаборатории фармакофорных циклических систем УфИХ УФИЦ РАН производных осуществлено с помощью компьютерной программы PASS. Проведены биологические испытания ЛГ и его производных.
Результаты. Впервые изучена острая токсичность ЛГ, выявлены цитотоксические, фунгистатические, бактериостатические, антиагрегационные, антикоагулянтные, антиоксидантные свойства ЛГ и его производных.
Ограничения исследования. Высокая стоимость биологических испытаний соединений.
Заключение. Безусловно, внимание исследователей к ЛГ оправдано его активированным для дальнейших превращений строением и биологической активностью как самой молекулы, так и её производных. Среди исследуемых соединений выявлены лидеры по биологической активности, при этом ЛГ и его производные являются хиральными органическими молекулами и представляют интерес для библиотек соединений с необходимым биологическим действием. Данная статья может представлять интерес для учёных, работающих в области поиска полученных из доступных природных объектов новых перспективных хиральных молекул с целью выявления их фармакологического потенциала и дальнейшего использования в медицине.
Соблюдение этических стандартов. Протокол № 8 семинара по органической и биоорганической химии Уфимского института химии УФИЦ РАН от 10.04.2025 г.
Вклад авторов:
Ахметдинова Н.П. – сбор материала и обработка данных, написание текста;
Файзуллина Л.Х. – концепция и дизайн исследования, редактирование;
Самородов А.В. – концепция и дизайн исследования, редактирование.
Все соавторы – утверждение окончательного варианта статьи и ответственность за целостность всех её частей.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов в связи с публикацией данной статьи.
Финансирование. Исследование поддержано государственным заданием Уфимского института химии УФИЦ РАН по теме «Разработка стратегий и методов целенаправленного синтеза практически важных веществ на основе фундаментальных исследований свойств природных соединений и продуктов органического синтеза» (государственная регистрация – № 125020601627-6).
Поступила: 23.04.2025 / Принята к печати: 02.12.2025 / Опубликована: 13.03.2026
Ключевые слова
Для цитирования:
Ахметдинова Н.П., Самородов А.В., Файзуллина Л.Х. Биологическая активность левоглюкозенона и его производных (аналитический обзор). Гигиена и санитария. 2026;105(2):207-213. https://doi.org/10.47470/0016-9900-2026-105-2-207-213. EDN: flrmmn
For citation:
Akhmetdinova N.P., Samorodov A.V., Faizullina L.Kh. Biological activity of levoglucosenone and its derivatives (analytical review). Hygiene and Sanitation. 2026;105(2):207-213. (In Russ.) https://doi.org/10.47470/0016-9900-2026-105-2-207-213. EDN: flrmmn
Введение
Левоглюкозенон [1,6-ангидро-3,4-дидезокси-β-D-пираноз-3-ен-2-он] (ЛГ) – енон углеводной природы, получаемый кислотным пиролизом целлюлозы, привлёк внимание исследователей своим высоким синтетическим потенциалом [1–5]. В нём удачно сочетаются 6,8-диоксабицикло[3.2.1]октановый каркас, сопряжённая еноновая система, активированные кетогруппа и ацетальный центр, что обеспечивает данному соединению высокую реакционную активность и надёжную стереоконтролируемую способность в реакциях получения ценных хиральных строительных блоков для природных соединений и их аналогов.
С учётом мощного синтетического потенциала и доступности ЛГ мы посчитали интересным изучить его возможности как платформы в синтезе широкого круга хиральных органических молекул с целью выявления биологической активности полученных производных.
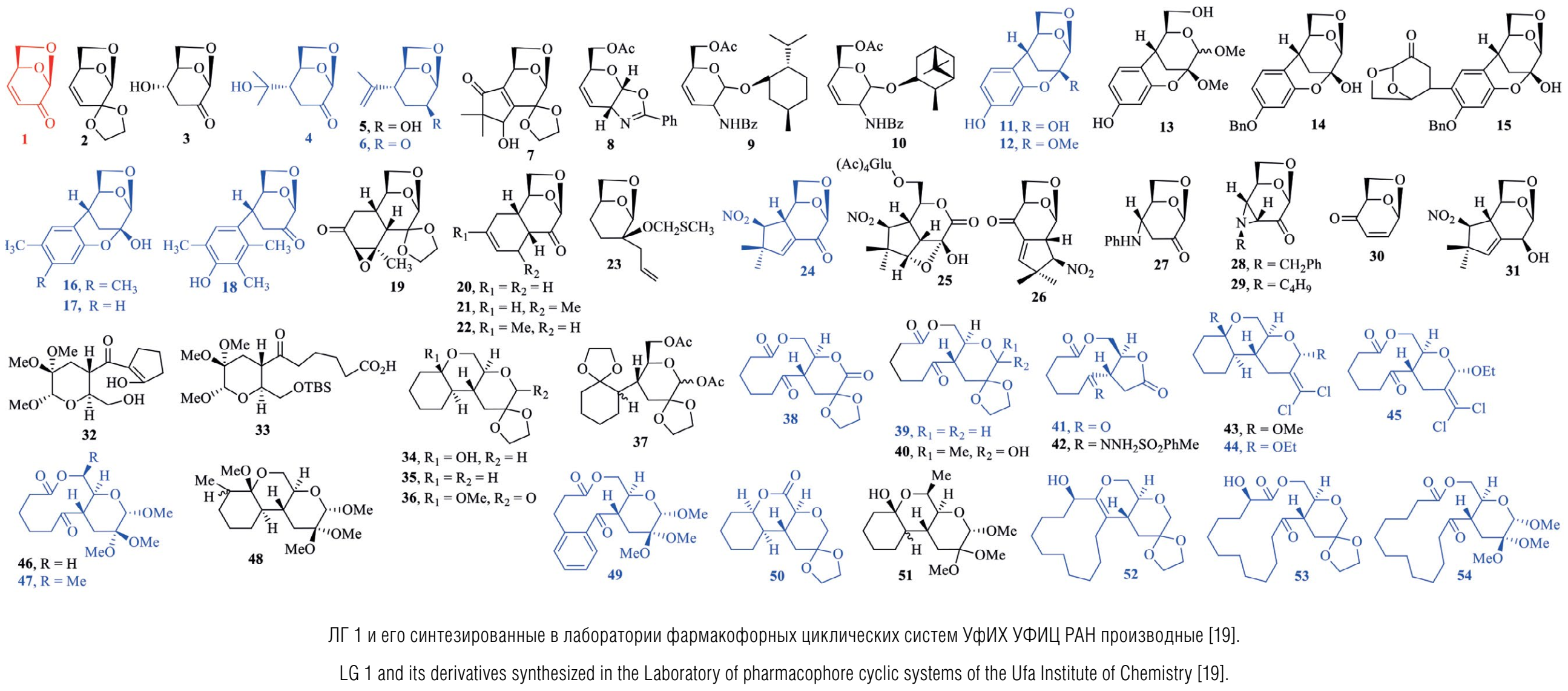
Сотрудниками лаборатории фармакофорных циклических систем УфИХ УФИЦ РАН было получено более 200 производных ЛГ, среди которых были выбраны 54 соединения, в том числе ЛГ 1, обладающих потенциально интересным биологическим действием (рисунок, см. на вклейке).
Материалы и методы
Прогнозирование спектра биологической активности ЛГ и его синтезированных производных проводили с помощью компьютерной системы PASS [6].
Экспериментальная работа по изучению острой токсичности ЛГ, антикоагуляционной, антиагрегационной, антиоксидантной активности ЛГ и его производных была проведена на кафедре фармакологии с курсом клинической фармакологии ФГБОУ ВО БГМУ Минздрава России в соответствии с рекомендациями «Руководства по доклиническому изучению новых фармакологических веществ» [7, 8].
Оценку антиагрегантной и антикоагулянтной активности проводили в условиях in vitro на крови 39 здоровых доноров-мужчин 18–24 лет. Изучали влияние соединений на максимальную амплитуду агрегации (МА), скорость агрегации и время достижения МА при агрегации тромбоцитов, индуцированной АДФ [9, 10]. В качестве препаратов сравнения использовали ацетилсалициловую кислоту.
Определение антикоагулянтной активности проводили клоттинговыми тестами на турбидиметрическом гемокоагулометре. Изучали показатели активированного парциального тромбопластинового времени (АПТВ), протромбинового времени (ПВ) и концентрации фибриногена по A. Clauss. В качестве препарата сравнения использовали гепарин натрия.
Скрининг антиокислительной активности соединений оценивали регистрацией хемилюминесценции (ХЛ). В качестве наиболее информативных показателей ХЛ использовали светосумму (S) и максимальную амплитуду медленной вспышки (Imax), результаты представлены в процентах от контроля [11–13].
Токсикологические исследования проводили на белых мышах-самцах в возрасте 2 мес со средней массой тела 20–21 г при внутрибрюшном введении. ЛГ исследовали в дозах 1; 10; 50; 100; 200; 300 мг/кг. Наблюдение за опытными группами проводилось в течение 14 сут. Результаты исследования обработаны с применением статистического пакета Statistica 10,0 (StatSoft Inc, США). Проверку на нормальность распределения фактических данных выполняли с помощью критерия Шапиро – Уилка. Выявлено, что вид распределения полученных данных отличается от нормального, поэтому при дальнейшей работе использовались непараметрические методы. Данные представлены в виде медианы, 25-го и 75-го процентилей. Дисперсионный анализ проводили с помощью U-критерия Манна – Уитни. Величину LD50 рассчитывали с помощью нелинейного фиттинга кривых, описывающих падёж животных (%) по логарифмическому уравнению с 4 параметрами, используя программное обеспечение GraphPad Prism (GraphPad Software, Inc., CШA).
Антиоксидантную активность также исследовали в лаборатории химической кинетики УфИХ УФИЦ РАН волюмометрическим методом на модели радикально-цепного окисления 1,4-диоксана [14].
Фунгистатическую и бактериостатическую активность изучали в лаборатории микробиологии УфИБ УФИЦ РАН. Оценку фунгицидной (по отношению к грибам Bipolaris sorokiniana, Fusarium oxysporum, Rhizoctonia solani) и противобактериальной (по отношению к бактериям Bacillus atrophaeus, B. subtilis, Pseudomonas frederiksbergensis, Р. mandelii, P. еxtremaustralis, Streptomyces atroolivaceus, S. xanthophaeus) активности соединений проводили in vitro методом диффузии в агар. Активность оценивали по диаметру зоны подавления роста микроорганизмов. В качестве растворителей использовали 0,5%-й раствор DMSO и 50%-й раствор ацетона, не оказывающие отрицательного влияния на развитие грибов и бактерий [15].
Цитотоксическая активность была изучена в Национальном институте рака (NCI) США в рамках соглашения между УфИХ РАН и NCI. Цитотоксическая активность против опухолевых клеток-мишеней исследована in vitro по отношению к клеткам 60 линий 9 различных опухолей человека (лёгкого, толстой кишки, центральной нервной системы, головного мозга, почки, яичника, простаты, лейкоза, меланомы) [16–18].
Авторы выражают искреннюю благодарность сотрудникам лаборатории химической кинетики УфИХ УФИЦ РАН за предоставленные результаты изучения антиоксидантной активности и сотрудникам лаборатории прикладной микробиологии УфИБ УФИЦ РАН за проведение исследований фунгистатической и бактериостатической активности.
Результаты
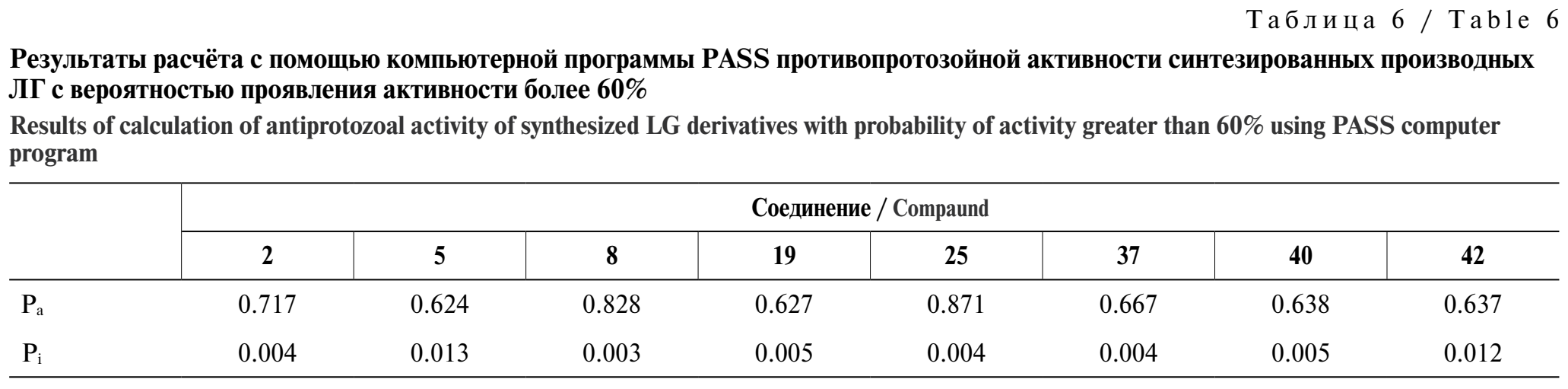
Расчёты, выполненные с помощью компьютерной программы PASS, указали на вероятность проявления у основной части исследуемых соединений более 70% противоопухолевой активности, в том числе в отношении рака молочной железы, яичников, лёгких, карциномы, лейкемии, у ряда соединений противовоспалительной, иммуносупрессивной, противоэрозийной активности, а также с вероятностью более 60% противогрибковой и противопротозойной активности (табл. 1–6).
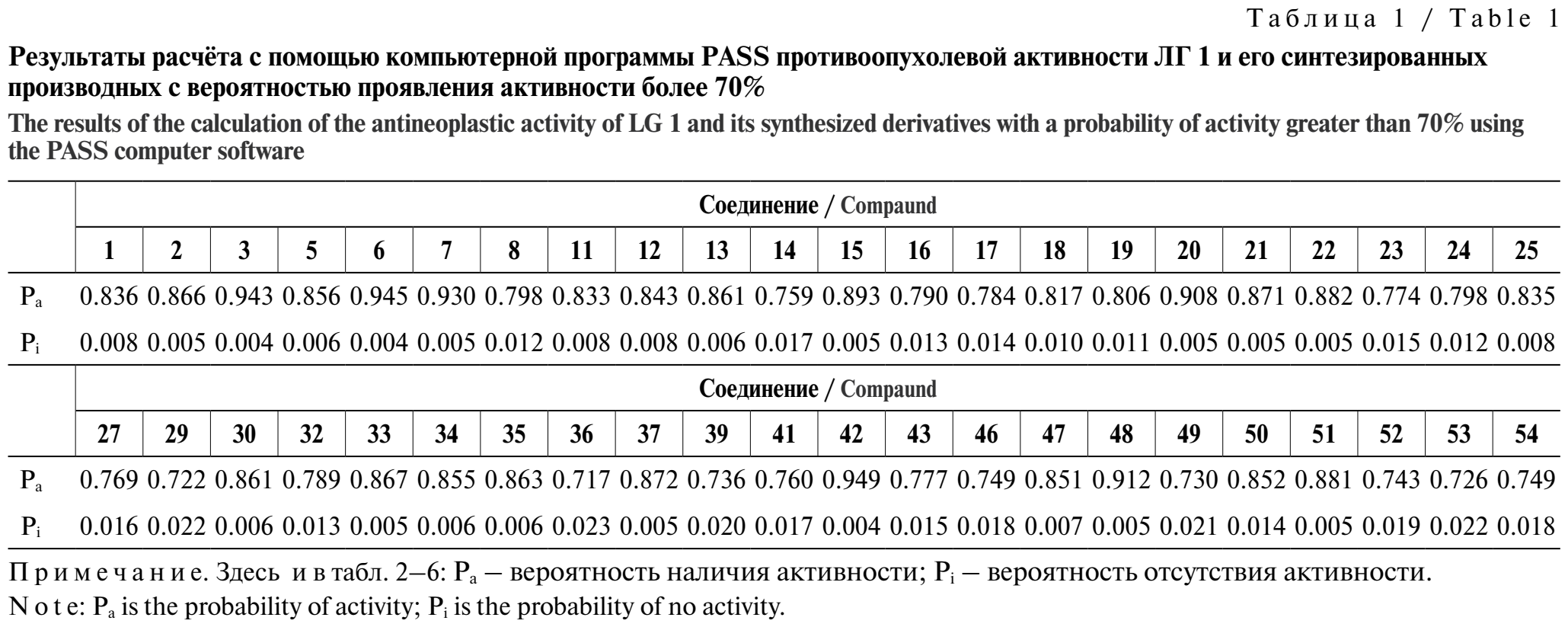
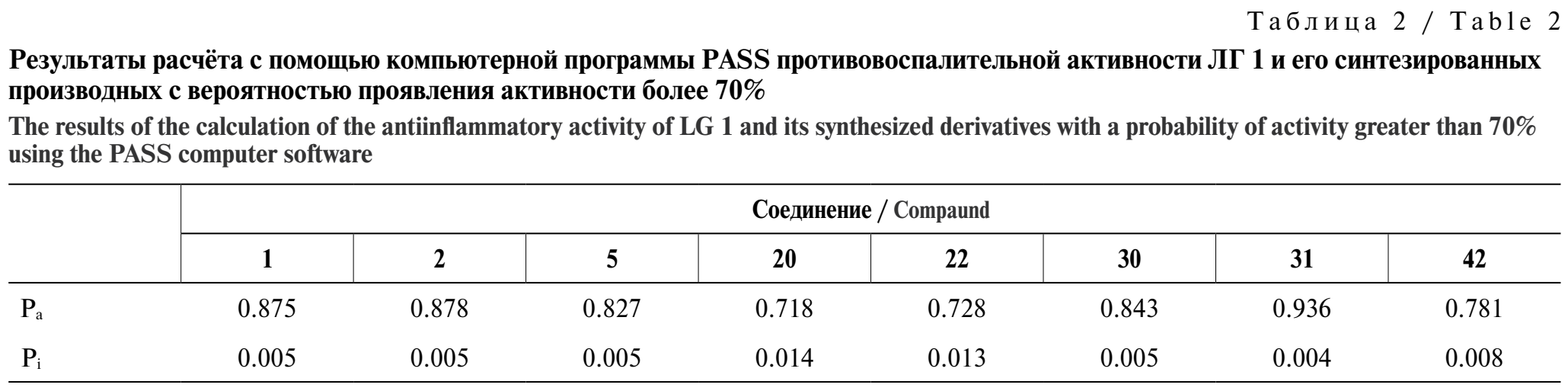

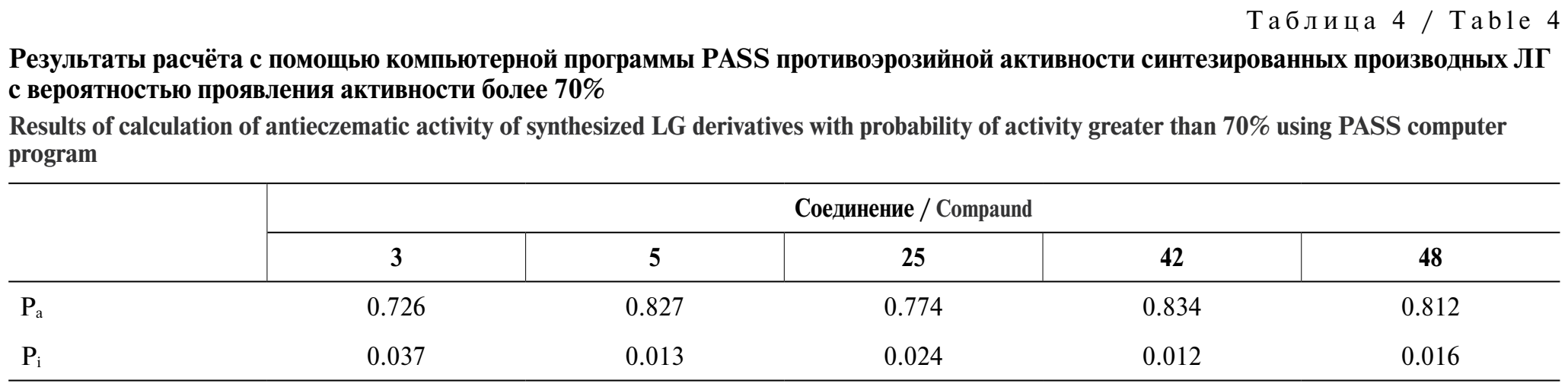

Для ЛГ и его синтезированных производных были проведены доступные нам биологические испытания. Исследована острая токсичность ЛГ 1, определены цитотоксическая, фунгистатическая, бактериостатическая, антиагрегационная, антикоагулянтная, антиоксидантная активность ЛГ и его производных.
Экспериментальное изучение острой токсичности при внутрибрюшинном введении мышам ЛГ показало значение LD50 = 46,8 мг/кг. При введении ЛГ в дозировках 1 и 10 мг/кг гибель мышей не регистрировалась, увеличение дозы до 50 мг/кг привело к заторможенному состоянию животных, сохранялась реакция на звуковые и тактильные раздражения, в течение 20 мин после введения вещества была отмечена гибель 40% животных. Увеличение доз до 100 и 200 мг/кг привело в первые минуты после введения вещества к тоническим судорогам, спазму мышц брюшной полости, гибели 100% мышей.
При наблюдении за выжившими мышами в последующие дни после введения вещества изменений в поведении не отмечено, мыши активно передвигались в клетке, реагировали на звуковые и тактильные раздражители, отсроченной гибели не зарегистрировано. Макроскопическое исследование погибших мышей показало: анатомический рисунок органов сохранён, печень полнокровна, головной мозг и внутренние органы брюшной полости оставались без изменения, в желудке видимых изменений не наблюдалось, в обеих долях лёгкого обнаружены множественные кровоизлияния.
В результате изучения фунгистатической и бактериостатической активности производных ЛГ соединения 3, 4, 5, 8, 11, 12, 24–29, 32, 35, 36, 38, 41–43, 45–47, 49, 52–54 показали высокую фунгистатическую активность в отношении Rhizoctonia solani, задерживая рост мицелия и формирование хламидоспор. Соединения 1, 6, 23 оказывали фунгицидное воздействие на R. solani, полностью подавляя рост и спороношение. Соединения 1, 12, 23, 27–29, 41, 42, 54 оказывали фунгистатическое действие на Bipolaris sorokiniana, соединения 1, 23, 28, 41, 54 оказывали фунгистатическое действие на Fusarium oxysporum.
Соединения 1, 54 оказывали бактериостатическое действие на Streptomyces xanthophaeus, S. atroolivaceus. Соединение 3 оказывало бактериостатическое действие на Pseudomonas frederiksbergensis, Р. mandelii, P. Еxtremaustralis. Cоединения 8, 24–27, 32, 38, 41, 43, 45, 47, 49, 53 оказывали умеренное негативное воздействие на рост Bacillus subtilis, B. atrophaeus, Pseudomonas mandelii.
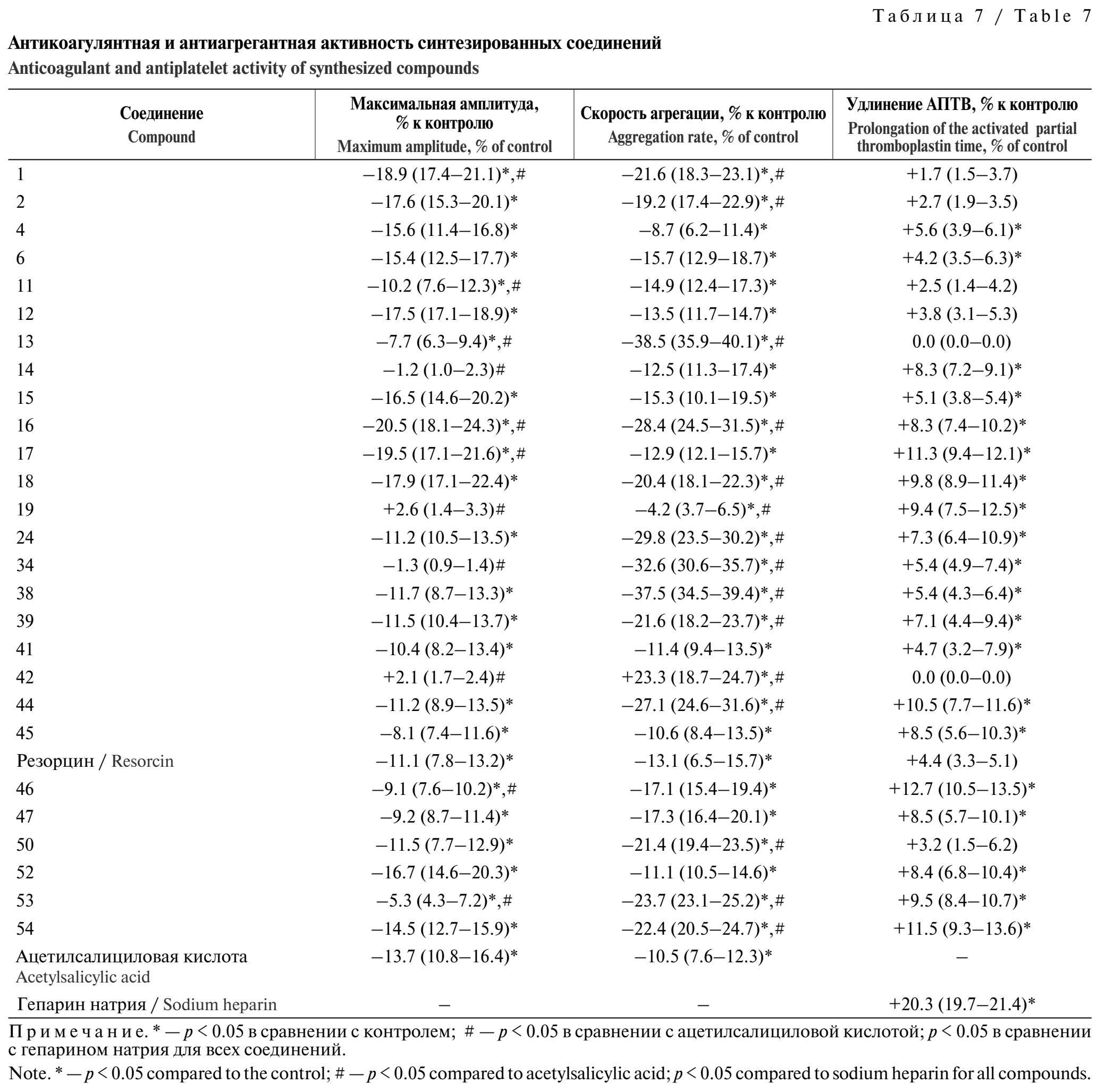
Результаты проведённых in vitro исследований антикоагуляционной и антиагрегационной активности производных ЛГ показали, что переданные на испытания соединения оказывали влияние различной степени выраженности на плазменный компонент системы гемостаза, проявляющееся изменением показателя внутреннего пути свёртывания крови – АПТВ. Исследуемые соединения не влияли на концентрацию фибриногена и ПВ. Наибольший антикоагуляционный потенциал фиксировали у соединений 17–19, 44, 46, 53, 54, повышающих АПТВ в среднем на 9,4–12,7% по сравнению с контролем, однако данные соединения уступали гепарину натрия, удлинявшему значения АПТВ в среднем на 20,3%. Остальные соединения вызывали гипокоагуляцию, повышая АПТВ на 1,7–8,5% по сравнению с контролем. По показателю максимальной амплитуды агрегации тромбоцитов соединения 1, 2, 12, 15–18, 52 проявляли антиагрегационную активность, превышающую показатели препарата сравнения (ацетилсалициловой кислоты), а соединения 4, 6, 11, 24, 38, 39, 41, 44, 45, 47, 50, 54 и резорцин проявляли антиагрегационную активность на уровне ацетилсалициловой кислоты. Скорость агрегации тромбоцитов уменьшалась для всех указанных производных, кроме соединения 42 (табл. 7).
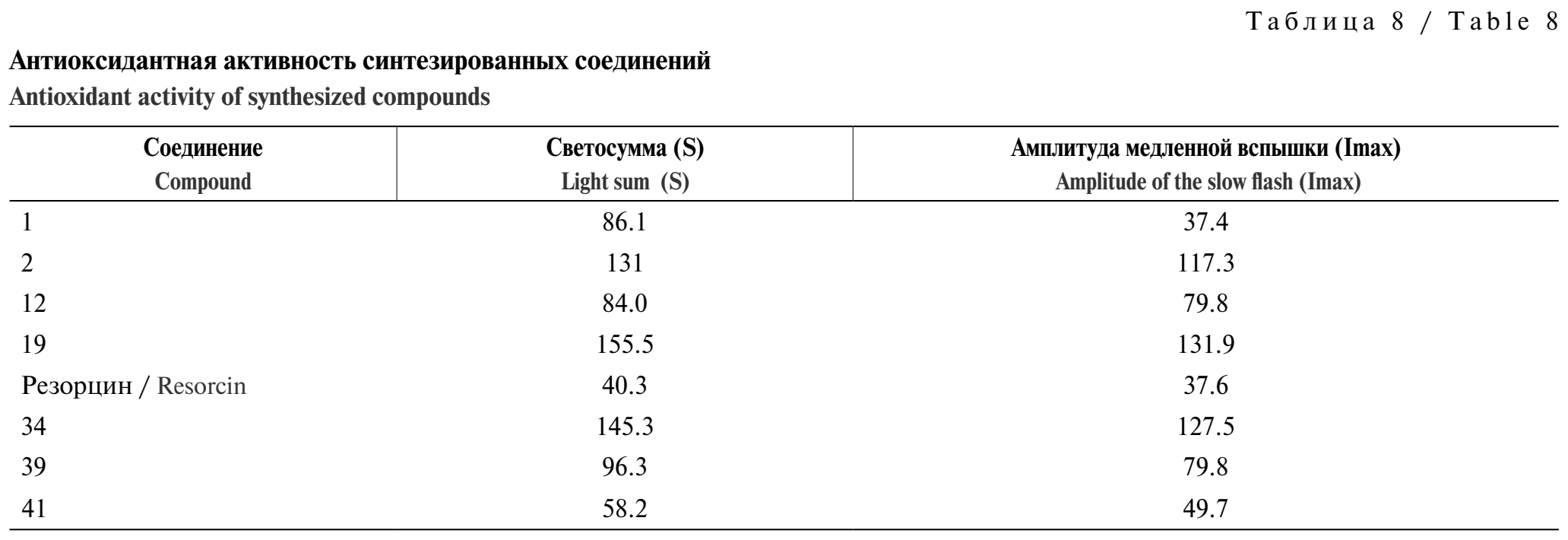
В результате изучения антиоксидантных свойств ЛГ и его производных установлено, что соединения 1, 12, 39, 41 проявили антиоксидантную активность, соединения 2, 19, 34 – прооксидантную активность (табл. 8).
Изучение влияния метильных заместителей в производных фенола 12, 16–18 на антиоксидантную активность проводили по скорости реакции данных соединений с пероксильными радикалами, образованными в ходе инициированного окисления 1,4-диоксана. Согласно полученным результатам, с увеличением концентрации соединений 12, 16–18 скорость окисления снижалась. Эффективную константу скорости реакции рассчитывали преобразованием зависимости скорости радикально-цепного окисления 1,4-диоксана от концентрации соединений 12, 16–18 в координатах уравнения [14, 15]. По результатам проведённых исследований установлено, что соединения 12, 16–18 проявили антиоксидантную активность, производное 18 стало лидером по величине эффективной константы скорости реакции, значение которой в два раза превышало рассчитанное в этих же условиях для известного ингибитора ионола [20] (табл. 9).

Проявили умеренные цитотоксические свойства 8 синтезированных производных ЛГ. В отношении клеток HL-60 (TB), MOLT-4, RPMI-8226 (лейкемия) обнаружена способность соединения 9 угнетать рост данных типов клеток на 26; 21; 15% соответственно, тогда как соединение 10 подавляло рост этих же клеток на 4; 11; 25% соответственно. Одновременно последние усиливали пролиферацию клеток: гликозид 9 DU-145 (рак простаты) – на 32%, OVCAR-4 (рак почек) – на 36%, гликозид 10 A498 (рак почек) – на 43%, MDA-MB-468 (рак молочной железы) – на 33%. Соединение 24 подавляло рост клеток MOLT-4 (лейкемия) на 26%, но при этом способствовало росту клеток NCI-H322M (рак лёгких) на 61%. Лактоны 41, 45 и 50 подавляли рост клеток SNB-75 (рак центральной нервной системы) на 23; 18; 22% соответственно, лактоны 47 и 49 к этим видам клеток не были чувствительны. Лактон 49 подавлял рост клеток UO-31 (рака почек) на 18%, а аналог форакантолида 47 угнетал рост клеток LOX IMVI (меланома) и A498 (рака почек) на 14 и 15% соответственно, но при этом способствовал росту клеток CCRF-CEM (лейкемия) и IGROV1 (рак яичников) на 27 и 26% соответственно.
Обсуждение
Профиль биологической активности соединений во многом определяется структурой молекулы. Первоначальное прогнозирование спектра биологической активности ЛГ и его синтезированных производных на основе их структурной формулы, проведённое с использованием компьютерной программы PASS, показало преобладание разнообразной противоопухолевой, в меньшей степени противовоспалительной, иммуносупрессивной, противопротозойной, противоэрозийной, противогрибковой, антиагрегационной активности. Для объективной оценки биологической активности и полного раскрытия фармакологического потенциала соединений целесообразно изучать взаимосвязь «структура – активность» с помощью биологических испытаний.
Циклическая еноновая группировка играет решающую роль в связывании активных форм кислорода, тем самым определяя профиль биологической активности молекулы ЛГ. В результате проведённых биологических испытаний выявлены антиагрегационная, фунгистатическая, бактериостатическая, антиоксидантная активность ЛГ.
При изучении биологической активности производных ЛГ выявлено, что наличие у соединений 17, 18 ароматического фрагмента с метильными заместителями способствует проявлению антикоагуляционной и антиагрегационной активности. Присутствие у производных 12, 18 замещённого фенольного фрагмента определяет антиоксидантную активность. Наличие гетероатомов (S, N) у производных 23, 28 или лактонного фрагмента у производных 41, 54 стимулирует проявление фунгистатического действия. Присутствие у производного 24 еноновой группировки, у производных 45, 47 лактонного фрагмента отвечает за проявление антиагрегационной, фунгистатической, бактериостатической, цитотоксической активности.
Среди изучаемого ряда соединений выявлены лидеры биологической активности, соединения 1, 3, 8, 24–27, 32, 41, 43, 45, 47, 49, 54 обладают одновременно фунгистатической и бактериостатической активностью; синтоны 1, 12, 16, 17, 18, 39 показали антиагрегационную и антиоксидантную активность; производные 24, 41, 45, 47, 50 проявили антиагрегационную и цитотоксическую активность.
Заключение
Левоглюкозенон – химически уникальная молекула с огромным потенциалом синтеза разнообразных хиральных соединений, привлекательных для изучения их биологических свойств. Полученные из ЛГ синтоны являются биологически активными и перспективны при синтезе практически значимых природных молекул, а также пополнении библиотек соединениями с необходимой биологической активностью.
В данной работе впервые изучена токсичность ЛГ. В соответствии с классификацией химических веществ по параметрам острой токсичности его можно отнести ко второму классу опасности. Выявлены цитотоксические, фунгистатические, бактериостатические, антиагрегационные, антикоагулянтные и антиоксидантные свойства ЛГ и его синтезированных производных. В результате проведённых биологических испытаний были определены перспективные соединения (1, 4, 6, 11, 12, 16–18, 24, 38, 39, 41, 44, 45, 47, 49, 50, 52–54), обладающие одновременно двумя и более видами биологической активности, полезные при лечении острых и хронических воспалений, рака, болезней крови, аутоиммунных, кожных и других патологий, активные в отношении ряда ДНК-, РНК-вирусов, в том числе HIV-1 и вируса гриппа.
Список литературы
1. Мифтахов М.С., Валеев Ф.А., Гайсина И.Н. Левоглюкозенон: свойства, реакции и использование в тонком органическом синтезе. Успехи химии. 1994; 63(10): 922–36. https://doi.org/10.1070/RC1994v063n10ABEH000123
2. Witczak Z.J. Levoglucosenone and Levoglucosans: Chemistry and Applications. ATL Press; 1994.
3. Witczak Z.J. Carbohydrate therapeutic: new developments and strategies. Carbohydr. Drug Des. 2006; 932: 25–46. https://doi.org/10.1021/bk-2006-0932.ch002
4. Sarotti A.M., Zanardi M.M., Spanevello R.A., Suarez A.G. Recent applications of levoglucosenone as chiral synthon. Curr. Org. Synth. 2012; 9(4): 439–59. https://doi.org/10.2174/157017912802651401
5. Comba M.B., Tsai Y.H., Sarotti A.M., Mangione M.I., Suárez A.G., Spanevello R.A. Levoglucosenone and its new applications: valorization of cellulose residues. Eur. J. Org. Chem. 2018; 2018(5): 590–604. https://doi.org/10.1002/ejoc.201701227 https://elibrary.ru/yghrql
6. Available at: https://www.way2drug.com/PassOnline/predict.php
7. Миронов А.Н., ред. Методические рекомендации по доклиническому изучению противоопухолевой активности лекарственных средств. Руководство по проведению доклинических исследований лекарственных средств. Часть 1. М.: Гриф и К; 2012: 642–56. https://elibrary.ru/sdewmp
8. Миронов А.Н., Бунатян Н.Д. Руководство по проведению доклинических исследований лекарственных средств. Часть 1. Москва: Гриф и К; 2012.
9. Гуревич К.Г., Ураков А.Л., Клен Е.Э., Самородов А.В., Никитина И.Л., Халиуллин Ф.А. и др. Синтез и биологическая активность этиловых эфиров 2-[8-арилметилиденгидразино-3-метил-7-(1-оксотиетанил-3)-ксантинил-1]уксусных кислот. Химико-фармацевтический журнал. 2020; 54(3): 3–10. https://doi.org/10.30906/0023-1134-2020-54-3-3-10 https://elibrary.ru/llowuk
10. Born G.V., Garrod D. Photometric demonstration of aggregation of slime mould cells showing effects of temperature and ionic strength. Nature. 1968; 220(5167): 616–8. https://doi.org/10.1038/220616a0
11. Faizullina L.Kh., Khalilova Yu.A., Valeev F.A., Pavlov V.N., Samorodov A.V. Preparation of the adduct of levoglucosenone and resorcinol and its in vitro antiplatelet and anticoagulant activity. Chem. Heterocycl. Comp. 2021; 57(9): 966–9. https://doi.org/10.1007/s10593-021-03007-0 https://elibrary.ru/mvrfke
12. Халиуллин Ф.А., Маматов Ж.К., Тимирханова Г.А., Самородов А.В., Баширова Л.И. Синтез, антиагрегационная и антиоксидантная активность солей 2-[(1-изо-бутил-3-метил-7-(тиетанил-3)ксантин-8-ил)тио]уксусной кислоты. Химико-фармацевтический журнал. 2020; 54(9): 9–14. https://doi.org/10.30906/0023-1134-2020-54-9-9-14 https://elibrary.ru/acvypx
13. Файзуллина Л.Х., Карамышева Л.Ш., Якупова Л.Р., Мигранов А.Р., Сафиуллин Р.Л., Валеев Ф.А. и др. Синтез и оценка антиоксидантной, антикоагуляционной и антиагрегационной активности аддуктов левоглюкозенона, содержащих метилзамещенные фенильные фрагменты. Химико-фармацевтический журнал. 2024; 58(6): 48–53. https://doi.org/10.30906/0023-1134-2024-58-6-48-53 https://elibrary.ru/trdsvg
14. Якупова Л.Р., Хайруллина В.Р., Герчиков А.Я., Сафиуллин Р.Л., Баймуратова Г.Р. Кинетические закономерности жидкофазного окисления 1,4-диоксана в присутствии ингибиторов. Кинетика и катализ. 2008; 49(3): 387–91. https://elibrary.ru/ikputr
15. Sharipov B.T., Davidova A.N., Valeev F.A., Ryabova A.S., Galimzyanova N.F. Synthesis and fungicidal activity of methylsulfanyl methyl esters of levoglucosenone derivatives. Chem. Heterocycl. Compd. 2019; 55(1): 31–7. https://doi.org/10.1007/s10593-019-02415-7 https://elibrary.ru/rzmfri
16. Grever M.R., Schepartz S.A., Chabner B.A. The National Cancer Institute: cancer drug discovery and development program. Semin. Oncol. 1992; 19(6): 622–38.
17. Boyd M.R., Paull K.D. Some practical considerations and applications of the National Cancer Institute in vitro anticancer drug discovery screen. Drug Dev. Res. 1995; 34(2): 91–109. https://doi.org/10.1002/ddr.430340203
18. Shoemaker R.H. The NCI60 human tumour cell line anticancer drug screen. Nat. Rev. Cancer. 2006; 6(10): 813–23. https://doi.org/10.1038/nrc1951
19. Файзуллина Л.Х. Левоглюкозенон – биовозобновляемая платформа в стереоконтролируемых синтезах и превращениях аминопроизводных и ∆3-аддуктов: Автореф. дисс. … д-ра хим. наук. Уфа; 2022.
20. Valgimigli L. Lipid peroxidation and antioxidant protection. Biomolecules. 2023; 13(9): 1291. https://doi.org/10.3390/biom13091291
Об авторах
Наталья Павловна АхметдиноваРоссия
Канд. хим. наук, науч. сотр. УфИХ РАН, 450054, Уфа, Россия
e-mail: breeze-o@yandex.ru
Александр Владимирович Самородов
Россия
Доктор мед. наук, профессор, гл. науч. сотр. ФГБНУ ВИЛАР, 117216, Москва, Россия
e-mail: AVSamorodov@gmail.com
Лилия Халитовна Файзуллина
Россия
Доктор хим. наук, доцент, вед. науч. сотр., зав. лаб. УфИХ РАН, 450054, Уфа, Россия
e-mail: sinvmet@anrb.ru
Рецензия
Для цитирования:
Ахметдинова Н.П., Самородов А.В., Файзуллина Л.Х. Биологическая активность левоглюкозенона и его производных (аналитический обзор). Гигиена и санитария. 2026;105(2):207-213. https://doi.org/10.47470/0016-9900-2026-105-2-207-213. EDN: flrmmn
For citation:
Akhmetdinova N.P., Samorodov A.V., Faizullina L.Kh. Biological activity of levoglucosenone and its derivatives (analytical review). Hygiene and Sanitation. 2026;105(2):207-213. (In Russ.) https://doi.org/10.47470/0016-9900-2026-105-2-207-213. EDN: flrmmn
JATS XML








































